题目内容
10.化学与生产、生活密切相关,下列说法正确的是( )| A. | 工业上以氯气和石灰乳为原料制备漂白粉 | |
| B. | 焰火的五彩缤纷是某些金属元素化学性质的展现 | |
| C. | 用活性炭为糖脱色和用臭氧白纸浆的原理相似 | |
| D. | 明矾作为净水剂,可以除去废水中的铜离子 |
分析 A.氢氧化钙与氯气反应生成氯化钙、次氯酸钙和水;
B.某些金属或它们的化合物在无色火焰中灼烧时使火焰呈现特征的颜色的反应;
C.活性炭利用吸附性漂白,臭氧利用强氧化性漂白;
D.铝离子水解生成的氢氧化铝胶体具有吸附性,能够除去水中悬浮颗粒;
解答 解:A.氢氧化钙与氯气反应生成氯化钙、次氯酸钙和水,故A正确;
B.某些金属或它们的化合物在无色火焰中灼烧时使火焰呈现特征的颜色的反应,焰色反应是某些金素元素的物理性质,故B错误;
C.活性炭利用吸附性漂白,臭氧利用强氧化性漂白,则漂白原理不同,故C错误;
D.铝离子水解生成的氢氧化铝胶体具有吸附性,能够除去水中悬浮颗粒,不能除去铜离子,故D错误;
故选:A.
点评 本题考查了物质的性质和用途,明确漂白粉的制备原理、焰色反应的概念、活性炭漂白原理、明矾净水原理是解题关键,题目难度不大,注意焰色反应属于元素的物理性质.

练习册系列答案
相关题目
20.根据元素周期律的知识,下列两者性质比较中,正确的是( )
| A. | 热稳定性:HF<HCl | B. | 金属性强弱:K<Na | ||
| C. | 酸性强弱:H3PO4<H2SO4 | D. | 碱性强弱:NaOH<Mg(OH)2 |
1.从某含有FeCl2、FeCl3、CuCl2的工业废液中回收铜并制备氯化铁晶体的流程如图:
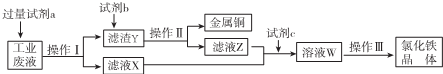
则下列说法正确的是( )

则下列说法正确的是( )
| A. | 试剂a是铁、试剂b是稀硫酸 | |
| B. | 试剂c是氯气,相应的反应为:2Fe2++Cl2═2Cl-+2Fe3+ | |
| C. | 操作I、操作Ⅱ、操作Ⅲ所用仪器相同 | |
| D. | 直接蒸干W溶液得到的氯化铁固体不含有结晶水 |
18.为比较Fe3+和Cu2+对H2O2分解的催化效果甲乙两组同学分别设计了如图一、图二所示的实验.下列说法正确的是( )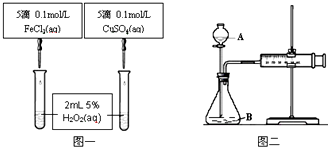

| A. | 图一可通过观察实验现象定量比较反应速率的大小 | |
| B. | 将CuSO4改为CuCl2更为合理 | |
| C. | 无法检查图二装置的气密性 | |
| D. | 图二所示实验中只需测量的数据是气体体积 |
5.表中有三组物质,每组都有一种物质与其他三种物质属于不同类别.请选出该物质,填在表相应的空格内.
| 序号 | 物质 | 被选出的 |
| (1) | O2、H2、C、N2 | C |
| (2) | Fe、Na、Al、Si | Si |
| (3) | NO、CO2、SO2、Fe3O4 | Fe3O4 |
15.常温下,向稀醋酸中不断加水稀释,始终保持不变的是( )
| A. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ | B. | $\frac{c(C{H}_{2}CO{O}^{-})}{c(C{H}_{3}COOH)}$ | ||
| C. | $\frac{c(O{H}^{-})}{c({H}^{+})}$ | D. | $\frac{c({H}^{+})•c(C{H}_{2}CO{O}^{-})}{c(C{H}_{3}COOH)}$ |
2.杀虫剂“阿乐丹”的结构简式为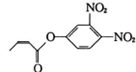 ,该分子中官能团(不含苯环)不含有( )
,该分子中官能团(不含苯环)不含有( )
 ,该分子中官能团(不含苯环)不含有( )
,该分子中官能团(不含苯环)不含有( )| A. | 酯基 | B. | 碳碳双键 | C. | 醚键 | D. | 硝基 |
19.下列有关化学反应速率的说法中,正确的是( )
| A. | 2mol/L盐酸与锌反应时,加入4mol/L的氯化钠溶液,生成氢气的速率加快 | |
| B. | 对于可逆反应2CO+2NO?N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快 | |
| C. | 工业上合成氨是放热反应,升高温度,正反应速率减慢 | |
| D. | 在K2SO4和BaCl2两溶液反应时,增大压强,生成沉淀速率加快 |
20.肼(N2H4)-空气燃料电池以KOH溶液为电解质溶液,装置如图所示.下列有关叙述正确的是( )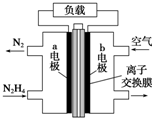

| A. | 放电时,电流从b极经过负载流向a极 | |
| B. | b极发生氧化反应 | |
| C. | a极的反应式为N2H4+4OH--4e-=N2+4H2O | |
| D. | 电池中的离子交换膜需选用阳离子交换膜 |