题目内容
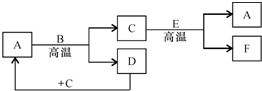 如图所示:已知A和E为金属单质,B是化合物且常温下为液态,F为两性化合物.
如图所示:已知A和E为金属单质,B是化合物且常温下为液态,F为两性化合物.按要求回答下列问题:
(1)E在元素周期表中位于第
(2)写出A和B反应的化学方程式:
(3)写出C和E反应的化学方程式:
(4)写出C和D反应的化学反应方程式为
考点:无机物的推断
专题:推断题
分析:B是化合物且常温下为液态,A为金属,二者在高温下反应得到C与D,且C具有磁性,C为Fe3O4,该反应为Fe和水的反应,所以A为Fe,B为H2O,D是H2,氢气可以与四氧化三铁反应置换得到Fe,金属E与四氧化三铁在高温下反应生成Fe与F,且F为两性化合物,该反应应为铝热反应,所以F为Al2O3,E为Al,据此解答.
解答:
解:B是化合物且常温下为液态,A为金属,二者在高温下反应得到C与D,且C具有磁性,该反应为Fe和水的反应,所以A为Fe,B为H2O,C为Fe3O4,D是H2,氢气可以与四氧化三铁反应置换得到Fe,金属E与四氧化三铁在高温下反应生成Fe与F,且F为两性化合物,该反应应为铝热反应,所以F为Al2O3,E为Al,
(1)E为Al,原子序数为13,原子核外有3个电子层,最外层电子数为3,则位于周期表第三周期ⅢA族,
故答案为:三;ⅢA;
(2)Fe和H2O在高温下反应生成Fe3O4和H2,反应的方程式为3Fe+4 H2O(g)
Fe3O4+4H2,
故答案为:3Fe+4 H2O(g)
Fe3O4+4H2;
(3)Al和Fe3O4在高温下发生铝热反应,反应的方程式为3Fe3O4+8Al
4Al2O3+9Fe,
故答案为:3Fe3O4+8Al
4Al2O3+9Fe;
(4)Fe3O4和H2在高温下反应生成Fe和H2O,反应的化学反应方程式为Fe3O4+4H2
3Fe+4H2O,
故答案为:Fe3O4+4H2
3Fe+4H2O.
(1)E为Al,原子序数为13,原子核外有3个电子层,最外层电子数为3,则位于周期表第三周期ⅢA族,
故答案为:三;ⅢA;
(2)Fe和H2O在高温下反应生成Fe3O4和H2,反应的方程式为3Fe+4 H2O(g)
| ||
故答案为:3Fe+4 H2O(g)
| ||
(3)Al和Fe3O4在高温下发生铝热反应,反应的方程式为3Fe3O4+8Al
| ||
故答案为:3Fe3O4+8Al
| ||
(4)Fe3O4和H2在高温下反应生成Fe和H2O,反应的化学反应方程式为Fe3O4+4H2
| ||
故答案为:Fe3O4+4H2
| ||
点评:本题考查无机物的推断,题目难度中等,答题是注意题目的突破口:“B是化合物且常温下为液态,C具有磁性,F为两性化合物”结合转化关系进行推断,掌握元素化合物知识是解答该类题目的关键.

练习册系列答案
相关题目
下列各组物质能用水鉴别的是( )
①NaCl、CaCO3 ②C2H5OH、苯、CCl4 ③NaOH、NaCl、NH4NO3 ④无水CuSO4、Na2CO3 ⑤Na2O2、Na2CO3、Al2S3、Mg3N2.
①NaCl、CaCO3 ②C2H5OH、苯、CCl4 ③NaOH、NaCl、NH4NO3 ④无水CuSO4、Na2CO3 ⑤Na2O2、Na2CO3、Al2S3、Mg3N2.
| A、①②⑤ | B、①③⑤ |
| C、①②④⑤ | D、①②③④⑤ |
人体最重要的供能物质是( )
| A、蛋白质 | B、糖类 |
| C、脂肪 | D、维生素 |
下列各类烃中,碳、氢两元素的质量比为一定值的是( )
| A、烷烃 | B、烯烃 | C、炔烃 | D、芳香烃 |
分子式C3H6Cl2的氯代烷分子中的一个氢原子被氯原子取代后,可得到两种同分异构体,则C3H6Cl2的名称是( )
| A、1,3-二氯丙烷 |
| B、1,1-二氯丙烷 |
| C、1,2-二氯丙烷 |
| D、2,2-二氯丙烷 |
下列说法中正确的是( )
| A、废电池必须集中处理的首要原因是回收其中的各种金属、石墨电极及塑料包装等 |
| B、向煤燃料中加入生石灰,可以减少二氧化硫对大气的污染 |
| C、氟利昂可以破坏臭氧层,从而导致温室效应 |
| D、绿色食品是指使用过化肥和农药生产出来的农副产品 |
在-50℃液氨中有2NH3(液)?NH4++NH2-的电离平衡关系,两离子的平衡浓度均为1×10-15mol/L,下列对-50℃时液氨的表达中正确的是( )
| A、离子积是1×10-15 |
| B、以液氨为溶剂的溶液中C(NH4+)一定等于 C(NH2-) |
| C、若液氨中放人NaNH2,其离于积不变 |
| D、此液氨中放人NH4C1,其离子积数值增加 |
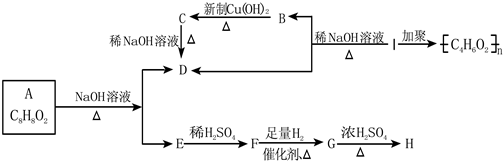 其中F能与FeCl3溶液显紫色,I为一种不饱和酯.
其中F能与FeCl3溶液显紫色,I为一种不饱和酯.