题目内容
6.表是元素周期表的一部分,回答下列有关问题:| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | Ⅷ |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)画出⑤原子的结构示意图:
 .
.③和⑧元素形成的化合物中含离子键键.(写化学键类型)
(3)在①--⑨的元素中,金属性最强的元素是Na,非金属性最强的元素是F,最不活泼的元素是Ar.(均用元素符号表示)
(4)⑧的最高价氧化物对应的水化物化学式是HClO4
(5)元素⑦与元素⑧相比,非金属性较强的是Cl>S(用元素符号表示),用一化学反应方程式表达这一事实Na2S+Cl2=S↓+2NaCl.
分析 (1)由元素在周期表中的位置可知,①为N,②为F,③为Na,④为Mg,⑤为Al,⑥为Si,⑦为S,⑧为Cl,⑨为Ar;
(2)⑤为Al,原子核外有13个电子,有3个电子层,各层电子数为2、8、3;
③和⑧元素形成的化合物为NaCl;
(3)同周期从左向右元素的金属性减弱、非金属性增强,同主族从上到下元素的金属性增强、非金属性减弱;稀有气体原子最外层为稳定结构,化学性质最不活泼;
(4)⑧的最高价氧化物对应的水化物为高氯酸;
(5)同周期从左向右元素的非金属性增强,可以利用单质之间的相互置换验证.
解答 解:(1)由元素在周期表中的位置可知,①为N,②为F,③为Na,④为Mg,⑤为Al,⑥为Si,⑦为S,⑧为Cl,⑨为Ar,故答案为:N;Si;
(2)⑤为Al,原子核外有13个电子,有3个电子层,各层电子数为2、8、3,原子结构示意图为: ;
;
③和⑧元素形成的化合物为NaCl,由活泼金属与活泼非金属性组成,含有离子键,
故答案为: ;离子键;
;离子键;
(3)同周期从左向右元素的金属性减弱、非金属性增强,同主族从上到下元素的金属性增强、非金属性减弱,上述元素中Na的金属性最强,F的非金属性最强,稀有气体Ar原子最外层为稳定结构,化学性质最不活泼,
故答案为:K;F;Ar;
(4)⑧的最高价氧化物对应的水化物为高氯酸,化学式为HClO4,故答案为:HClO4;
(5)同周期自左而右非金属性增强,故非金属性Cl>S,可以利用单质之间的相互置换进行验证,相应方程式为Na2S+Cl2=S↓+2NaCl,
故答案为:Cl>S;Na2S+Cl2=S↓+2NaCl.
点评 本题考查元素周期表与元素周期律,侧重对元素周期律的考查,注意理解掌握金属性、非金属性强弱比较及实验事实.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列叙述正确的是( )
| A. | 原子晶体的熔点一定比金属晶体的高 | |
| B. | 分子晶体的熔点一定比金属晶体的低 | |
| C. | 晶体内部的微粒按一定规律周期性的排列 | |
| D. | 凡有规则外形的固体一定是晶体 |
17.下列说法不正确的是( )
| A. | Na2O2能与CO2反应,可用作呼吸面具的供氧剂 | |
| B. | 硅是半导体材料,可用于制备光导纤维 | |
| C. | 明矾能水解生成Al(OH)3胶体,可用作净水剂 | |
| D. | Al2O3熔点高,可用于制作耐高温仪器 |
14.下列实验装置与叙述正确的是( )
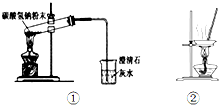

| A. | 用图①所示装置做碳酸氢钠固体受热分解实验 | |
| B. | 用装置②蒸干氯化镁溶液制MgCl2•6H2O | |
| C. | 锥形瓶可用作加热的反应器,滴定时不得用待测溶液润洗 | |
| D. | 配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏低 |
1.相同质量的两份铝,分别放入足量的盐酸和氢氧化钠溶液中,放出的氢气在同温同压下的体积之比为( )
| A. | 3:2 | B. | 2:3 | C. | 1:3 | D. | 1:1 |
11.下列各组物质中,都是强电解质的是( )
| A. | HBr、Cu(OH)2、BaSO4 | B. | NaOH、Ca(OH)2、NH3•H2O | ||
| C. | HClO、NaF、Ba(OH)2 | D. | NH4Cl、CH3COONa、Na2S |