题目内容
2.已知KHC2O4溶液显酸性,向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是( )| A. | c(K+)=c(HC2O4-)+c(H2C2O4)+2c(C2O42-) | B. | c(Na+)=c(H2C2O4)+c(C2O42-) | ||
| C. | c(K+)+c(Na+)=c(HC2O4-)+c(C2O42-) | D. | c(K+)>c(Na+) |
分析 HC2O4-既能够电离也能够水解,KHC2O4溶液显酸性,说明HC2O4-的电离程度大于水解程度;
A.根据物料守恒判断;
B.根据电荷守恒判断;
C.根据物料守恒、电荷守恒判断;
D.若恰好反应,c(K+)=c(Na+),此时溶液呈碱性,故加入的氢氧化钠的物质的量略少些;
解答 解:HC2O4-既能够电离也能够水解,KHC2O4溶液显酸性,说明HC2O4-的电离程度大于水解程度,根据电荷守恒与物料守恒得出结论;
A.碳元素在溶液中存在形式有:HC2O4-、H2C2O4、C2O42-,根据物料守恒有c(K+)=c(HC2O4-)+c(H2C2O4)+c(C2O42-),故A错误;
B.根据电荷守恒有:c(K+)+c(Na+)+c(H+)=c(HC2O4-)+2c(C2O42-)+c(OH-),溶液呈中性,则c(H+)=c(OH-),故c(K+)+c(Na+)=c(HC2O4-)+2c(C2O42-),故B错误;
C.由c(K+)=c(HC2O4-)+c(H2C2O4)+c(C2O42-)、c(K+)+c(Na+)=c(HC2O4-)+2c(C2O42-)可知,c(Na+)=c(C2O42-)-c(H2C2O4),故C错误;
D.若恰好反应,c(K+)=c(Na+),此时溶液呈碱性,故加入的氢氧化钠的物质的量略少些,故c(K+)>c(Na+),故D正确;
故选D.
点评 本题通过草酸考查了多元弱酸的电离方程式书写、电解质溶液中的电荷守恒和物料守恒,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.有关物质性质的比较,错误的是( )
| A. | 熔点:纯铁>生铁 | B. | 密度:硝基苯>水 | ||
| C. | 热稳定性:小苏打<苏打 | D. | 碳碳键键长:乙烯>苯 |
13.根据下列实验及现象,下列能量关系正确的是实验及现象能量关系( )
| 选项 | 实验及现象 | 能量关系 |
| A | 将盛“NO2玻璃球”置热水中,红棕色加深 | N2O4(g)?2NO2(g) △H<0 |
| B | NaOH与HCl溶液混合,溶液温度升高 | 反应物的能量>生成物的能量 |
| C | 钠投入水中,熔化成小球 | 反应物的能量<生成物的能量 |
| D | 微热含酚酞的Na2CO3溶液,溶液红色加深 | CO32-+H2O?HCO3-+OH-△H<0 |
| A. | A | B. | B | C. | C | D. | D |
10.下列实验中,对应的现象及结论都正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向某溶液中滴加氯水后再加入KSCN溶液 | 溶液呈红色 | 溶液中一定含有Fe2+ |
| B | 等体积pH=3的HA和HB两种酸分别与足量的锌反应 | 相同时间内HA与Zn反应生成的氢气更多 | HA是强酸 |
| C | 加热盛有NH4Cl固体的试管, | 试管底部固体消失,试管口有晶体凝结 | NH4Cl固体可以升华 |
| D | 向NaBr溶液中滴入少量氯水和苯,振荡、静置, | 溶液上层呈橙红色 | Br-还原性强于Cl- |
| A. | A | B. | B | C. | C | D. | D |
17.一种以NaBH4和H2O2为原料的新型电池的工作原理如图所示.下列说法错误的是( )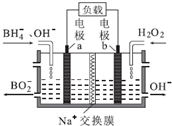

| A. | 电池的正极反应为H2O2+2e-=2OH- | |
| B. | 电池放电时Na+从a极区移向b极区 | |
| C. | 电子从电极b经外电路流向电极a | |
| D. | b极室的输出液经处理后可输入a极室循环利用 |
7.向含有下列微粒的溶液中分别加入少量NaOH固体、少量浓盐酸或少量酸性高锰酸钾溶液,都能使该微粒浓度下降的是( )
| A. | Fe3+ | B. | HS- | C. | 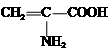 | D. | C6H5O- |
14.室温下,pH相同体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )
| A. | 加水稀释2倍后,两溶液的pH均减小 | |
| B. | 使温度都升高20℃后,两溶液的pH均不变 | |
| C. | 加适量的醋酸钠晶体后,盐酸pH增大,醋酸pH不变 | |
| D. | 加足量的锌充分反应后,醋酸产生的氢气比盐酸多 |
11.下列离子方程式错误的是( )
| A. | NaHSO3溶液显酸性是因为:HSO3-+H2O?SO32-+H3O+ | |
| B. | 尼泊金酸(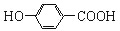 )与碳酸氢钠溶液反应: )与碳酸氢钠溶液反应: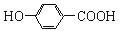 +2HCO3-→ +2HCO3-→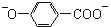 +CO2↑+2H2O +CO2↑+2H2O | |
| C. | KAl(SO4)2溶液中加入少量氢氧化钠溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | 足量硫酸氢钠溶液与氢氧化钡溶液混合:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
19.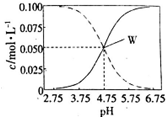 室温条件下在醋酸、醋酸钠混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol.L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关叙述正确的是( )
室温条件下在醋酸、醋酸钠混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol.L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关叙述正确的是( )
 室温条件下在醋酸、醋酸钠混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol.L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关叙述正确的是( )
室温条件下在醋酸、醋酸钠混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol.L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关叙述正确的是( )| A. | pH=5.5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | 向W点所表示的1.0L溶液中通人0.05molHCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-) | |
| C. | W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH)- | |
| D. | pH=3.5的溶液中:c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol.L-l |