题目内容
6.下列反应中,既属于氧化还原反应又属于置换反应的是( )| A. | CuCl2+2NaOH═Cu(OH)2↓+2NaCl | B. | CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$CO2+Cu | ||
| C. | Mg+2HCl═MgCl2+H2↑ | D. | Cl2+H2O═HCl+HClO |
分析 含元素化合价变化的反应为氧化还原反应,且单质与化合物反应生成新单质、化合物的反应为置换反应,以此来解答.
解答 解:A.不含元素的化合价变化,为非氧化还原反应,故A不选;
B.C、Cu元素的化合价变化,为氧化还原反应,但不属于置换反应,故B不选;
C.Mg、H元素的化合价变化,为氧化还原反应,且属于置换反应,故C选;
D.Cl元素的化合价变化,为氧化还原反应,但不属于置换反应,故D不选;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化及反应的分类为解答的关键,侧重氧化还原反应判断及分析与应用能力的考查,题目难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
17.如表是周期表中的一部分,根据A-E在周期表中的位置,按题目要求回答.
(1)B、C、D三元素的原子半径最大的是Na>Mg>Al(填元素符号)
(2)A、E两元素的氢化物中最稳定的是HF(填化学式);
(3)C元素的最高价氧化物的化学式是MgO;
(4)B的最高价氧化物的水化物和D的最高价氧化物相互反应的离子方程式Al2O3+2OH-=2AlO2-+H2O.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅧA | 0 |
| 1 | ||||||||
| 2 | A | |||||||
| 3 | B | C | D | E |
(2)A、E两元素的氢化物中最稳定的是HF(填化学式);
(3)C元素的最高价氧化物的化学式是MgO;
(4)B的最高价氧化物的水化物和D的最高价氧化物相互反应的离子方程式Al2O3+2OH-=2AlO2-+H2O.
14.意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子.已知N5是可用作烈性炸药的一种分子,下列关于N4、N5的说法正确的是( )
| A. | 相同质量的N4、N5分子其原子数之比为5:4 | |
| B. | N5、N4与N2互为同素异形体 | |
| C. | N4、N5均属于新型的化合物 | |
| D. | N5的摩尔质量为70 |
1.下列物质的贮存方法不正确的是( )
| A. | 新制氯水应保存在棕色瓶中 | B. | 少量金属钠保存在煤油中 | ||
| C. | 漂白粉可露置于空气中保存 | D. | 液溴采用液封法保存 |
11.下列化合物中,既有离子键,又有共价键的是( )
| A. | NaOH | B. | NH3 | C. | CaCl2 | D. | HCl |
18.下列各组离子在水溶液中一定能大量共存的是( )
| A. | 将铝粉投入溶液中会产生氢气:Mg2+、NO3-、K+、SO42- | |
| B. | 滴加石蕊试液会使溶液变蓝:Na+、Al3+、CO32-、NO3- | |
| C. | 将锌粒投入溶液中会产生氢气:Ca2+、Cl-、Mg2+、NH4+ | |
| D. | 溶液能使淀粉碘化钾试纸变蓝NH4+、CO32-、Cl-、SO32- |
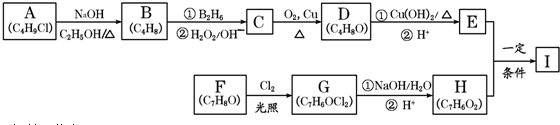
 ,该反应类型为取代反应.
,该反应类型为取代反应. .
. .
.