题目内容
14.某主族元素R的最高正化合价与最低负化合价的代数和为4,由此可以判断( )| A. | R一定有4个电子层 | |
| B. | R原子的最外层电子数一定为6 | |
| C. | R的气态氢化物比电子层数相同的其他非金属元素的气态氢化物稳定 | |
| D. | R气态氢化物化学式为H2R |
分析 设主族元素R的最高正化合价为x,则最低负价x-8,故有x+(x-8)=4,解得x=+6,该元素处于ⅥA族,以此解答该题.
解答 解:设主族元素R的最高正化合价为x,则最低负价x-8,故有x+(x-8)=4,解得x=+6,该元素处于ⅥA族,
A.不一定为第四周期元素,则不一定有4个电子层,故A错误;
B.由以上分析可知,R原子的最外层电子数一定为6,故B正确;
C.R为ⅥA族元素,非金属性比同周期ⅦA族弱,则气态氢化物较ⅦA族弱,故C错误;
D.R的最低负化合价为-2,氢化物化学式为H2R,故D正确.
故选BD.
点评 本题考查原子结构与元素周期律,为高频考点,侧重于学生的分析能力的考查,关键是清楚元素的最高价和最低负价的关系,难度不大.

练习册系列答案
相关题目
4.下列实验装置能达到实验目的是( )
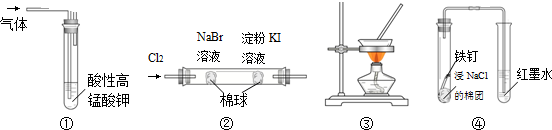

| A. | 图①装置可用于除去甲烷中混有的乙烯 | |
| B. | 图②装置可证明氧化性:Cl2>Br2>I2 | |
| C. | 图③装置可通过蒸干AlCl3饱和溶液制备AlCl3晶体 | |
| D. | 图④装置可观察铁的吸氧腐蚀 |
5.下列化学用语表达正确的是( )
| A. | HF的电子式为: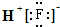 | |
| B. | HClO的结构式:H-Cl-O | |
| C. | 质子数为92、中子数为146的U原子:${\;}_{92}^{146}$U | |
| D. | Cl-的结构示意图: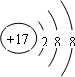 |
2.用石墨作电极,电解1mol•L-1下列物质的溶液,溶液pH变大的是( )
| A. | HCl | B. | H2SO4 | C. | NaCl | D. | Na2SO4 |
1.用石墨作电极,电解1mol•L-1下列物质的溶液,则电解前后溶液的pH保持不变的是( )
| A. | H2SO4 | B. | NaOH | C. | Na2SO4 | D. | NaCl |
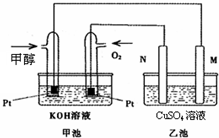 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇和水,并开发出以甲醇为燃料的燃料电池.已知图甲池为甲醇燃
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇和水,并开发出以甲醇为燃料的燃料电池.已知图甲池为甲醇燃