题目内容
13.己烷雌酚的一种合成路线如图,下列叙述正确的是( )
| A. | 在一定条件,化合物 Y 可与 HCHO 发生缩聚反应 | |
| B. | 用 FeCl3溶液不能鉴别化合物 X 和 Y | |
| C. | 在 NaOH 水溶液中加热,化合物 X 可发生消去反应 | |
| D. | 化合物 Y 中不含有手性碳原子 |
分析 A.Y含有酚羟基,与苯酚性质相似;
B.Y含有酚羟基,可与氯化铁发生显色反应;
C.X为卤代烃,在氢氧化钠水溶液中发生水解反应生成醇;
D.根据手性碳原子的定义判断.
解答 解:A.Y含有酚羟基,与苯酚性质相似,可与甲醛发生缩聚反应,故A正确;
B.Y含有酚羟基,可与氯化铁发生显色反应,可鉴别,故B错误;
C.X为卤代烃,在氢氧化钠水溶液中发生水解反应生成醇,如发生消去反应,条件为氢氧化钠醇溶液,故C错误;
D.连接四个不同的原子或原子团的碳原子为手性碳原子,Y中连接乙基的碳原子为手性碳原子,故D错误.
故选A.
点评 本题为2015年江苏考题第12题改编题,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,为解答该类题目的关键,难度不大.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
3. 有A、B、C、D、E五种元素,其相关信息如表:
有A、B、C、D、E五种元素,其相关信息如表:
请回答下列问题:
(1)写出E元素原子基态时的电子排布式1s22s22p63s23p63d104s1.
(2)C元素的第一电离能比氧元素的第一电离能大(填“大”或“小”).
(3)CA3分子中C原子的杂化类型是sp3.
(4)A、C、E三种元素可形成[E(CA3)4]2+,其中存在的化学键类型有①③(填序号);
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为a(填序号).
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)B与D可形成离子化合物,其晶胞结构如图所示.其中D离子的配位数为8,若该晶体的密度为a g•cm-3,则该晶胞的体积是$\frac{\frac{78}{{N}_{A}}×4}{a}$ cm3(写出表达式即可).
 有A、B、C、D、E五种元素,其相关信息如表:
有A、B、C、D、E五种元素,其相关信息如表:| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C基态原子的2p轨道中有3个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层 上有2个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
(1)写出E元素原子基态时的电子排布式1s22s22p63s23p63d104s1.
(2)C元素的第一电离能比氧元素的第一电离能大(填“大”或“小”).
(3)CA3分子中C原子的杂化类型是sp3.
(4)A、C、E三种元素可形成[E(CA3)4]2+,其中存在的化学键类型有①③(填序号);
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为a(填序号).
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)B与D可形成离子化合物,其晶胞结构如图所示.其中D离子的配位数为8,若该晶体的密度为a g•cm-3,则该晶胞的体积是$\frac{\frac{78}{{N}_{A}}×4}{a}$ cm3(写出表达式即可).
1.硅作为一种新型能源被广泛开发利用,关于其有利因素的下列说法中,你认为不正确的是( )
| A. | 硅燃烧产物对环境产生的污染,容易得到有效控制 | |
| B. | 硅燃烧可以放出较多的热量 | |
| C. | 自然界中硅的贮存量丰富,可以从自然界直接获得单质硅 | |
| D. | 硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料之一 |
8.下列离子方程式书写正确的是( )
| A. | NaHCO3溶液中加入稀 HCl:CO23-+2H+═H2O+CO2↑ | |
| B. | 将 NaHSO4与 Ba(OH)2溶液混合至中性:2H++SO24-+Ba2++2OH-═BaSO4↓+2H2O | |
| C. | 苯酚钠溶液中通入少量 CO2气体:2C6H5O-+CO2+H2O→2C6H5OH+CO23- | |
| D. | 用惰性电极电解氯化铝溶液:2Cl-+2H2O═Cl2↑+H2↑+2OH- |
5. Ⅰ.控制变量法是化学实验的一种常用方法.如表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
Ⅰ.控制变量法是化学实验的一种常用方法.如表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
(1)化学反应速率本质上是由反应物本身的性质决定的,但外界条件也会影响反应速率的大小.本实验中实验2和实验3表明温度对反应速率有影响,该因素对反应速率的具体影响是:其它条件相同时,温度越高反应速率越快.
(2)我们最好选取实验1、2和4(填3个实验序号)研究锌的形状对反应速率的影响.我们发现在其它条件相同时,反应物间的接触面积越大反应速率越快.
(3)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快.原因是锌会置换出少量的金属铜,在该条件下构成了原电池,加快了反应速率.
(4)利用表中数据,可以求得:硫酸的物质的量浓度是2.0mol/L.
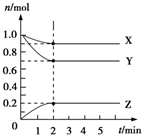
Ⅱ.某温度时,在5L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.请通过计算回答下列问题:
(5)反应开始至2min,Y的平均反应速率0.03mol/(L•min).
(6)分析有关数据,写出X、Y、Z的反应方程式X(g)+3Y(g)?2Z(g).
 Ⅰ.控制变量法是化学实验的一种常用方法.如表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
Ⅰ.控制变量法是化学实验的一种常用方法.如表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:| 序号 | 硫酸的体积/mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
| 1 | 50.0 | 2.0 | 薄片 | 25 | 100 | m1 |
| 2 | 50.0 | 2.0 | 颗粒 | 25 | 70 | m2 |
| 3 | 50.0 | 2.0 | 颗粒 | 35 | 35 | m3 |
| 4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
| 5 | 50.0 | 6.0 | 粉末 | 35 | 30 | m5 |
| 6 | 50.0 | 8.0 | 粉末 | 25 | t6 | 16.1 |
| 7 | 50.0 | 10.0 | 粉末 | 25 | t7 | 16.1 |
(2)我们最好选取实验1、2和4(填3个实验序号)研究锌的形状对反应速率的影响.我们发现在其它条件相同时,反应物间的接触面积越大反应速率越快.
(3)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快.原因是锌会置换出少量的金属铜,在该条件下构成了原电池,加快了反应速率.
(4)利用表中数据,可以求得:硫酸的物质的量浓度是2.0mol/L.
Ⅱ.某温度时,在5L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.请通过计算回答下列问题:
(5)反应开始至2min,Y的平均反应速率0.03mol/(L•min).
(6)分析有关数据,写出X、Y、Z的反应方程式X(g)+3Y(g)?2Z(g).
2.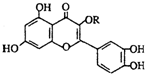 唐山市的市树是国槐,天然维生素P(结构如图)存在于国槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述正确的是( )
唐山市的市树是国槐,天然维生素P(结构如图)存在于国槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述正确的是( )
 唐山市的市树是国槐,天然维生素P(结构如图)存在于国槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述正确的是( )
唐山市的市树是国槐,天然维生素P(结构如图)存在于国槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述正确的是( )| A. | 若R为甲基则该物质的分子式可以表示为C16H10O7 | |
| B. | 分子中有三个苯环 | |
| C. | lmol该化合物与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4 mol、8 mol | |
| D. | lmol该化合物最多可与2molBr2完全反应 |
3.下列各组物质中,互为同素异形体的是( )
| A. | CH4和CH3CH3 | B. | 11H和 12H | C. | O2和O3 | D. | D2O和T2O |
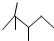 ,有机物 B 与等物质的量的 H2发生加成反应可得到有机物 A.则:
,有机物 B 与等物质的量的 H2发生加成反应可得到有机物 A.则: