题目内容
19.某元素R的核内含有N个中子,R的质量数为A,在其与氢化合时,R呈-n价,则WgR的气态氢化物中所含电子的物质的量为( )| A. | $\frac{A}{W+n}$(N-m)mol | B. | $\frac{W}{A+n}$(N+n)mol | C. | $\frac{W}{A+n}$(A-N+n)mol | D. | $\frac{W}{A+n}$(N-A-n)mol |
分析 本题根据原子的质量数=质子数+中子数,质子数=核外电子数,形成负价离子后,离子的核外电子数要加相应的价电子数,物质的量=物质的质量÷物质的相对分子质量来解题.
解答 解:元素R原子中含有电子数=质子数=质量数-中子数=A-N,形成氢化物是R得到n个电子,呈-n价,R离子中电子数为A-N+n,氢化物的相对分子质量为A+n,W g氢化物的物质的量为$\frac{W}{A+n}$ mol,
故氢化物中电子数为$\frac{W}{A+n}$(A-N+n)mol.
故选C.
点评 本题考查了原子的表示方法和物质的量的相关计算,综合性较强,明确质量数=质子数+中子数,质子数=核外电子数,离子的核外电子数=原子的核外电子数+价电子数是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列推断正确的是( )
| A. | SiO2 是酸性氧化物,能与NaOH溶液反应 | |
| B. | Na2O、Na2O2组成元素相同,与 CO2反应产物也相同 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 通过化学变化可以实现16O与18O间的相互转化 |
7.熟石灰的化学式是( )
| A. | Ca(OH)2 | B. | CaSO4 | C. | CaO | D. | CaCO3 |
11.下列物质能使溴的四氯化碳溶液发生反应褪色的是( )
| A. | 甲烷 | B. | 乙烷 | C. | 乙烯 | D. | 苯 |
8.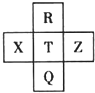 元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
 元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A. | 非金属性:Z<T<X | |
| B. | X最高价氧化物的水化物的表达式为H2XO4 | |
| C. | 气态氢化物稳定性:R<T<Q | |
| D. | R与Q的电子数相差26 |
9.下列搭配错误的是( )
| A. | 阿伏伽德罗常数----N | B. | 物质的量-----n | ||
| C. | 气体摩尔体积------Vm | D. | 物质的量浓度----CB |

 ;
; .
. .
.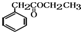 )的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
)的合成路线流程图(无机试剂任选).合成路线流程图示例如下: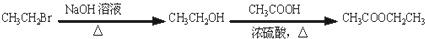
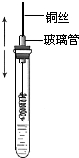 某同学在学习乙醇的知识后,设计了如下的实验. 操作步骤为:
某同学在学习乙醇的知识后,设计了如下的实验. 操作步骤为: ④
④ ⑤
⑤ ⑥
⑥
 ⑧
⑧ ⑨CH3-CH═CH2⑩
⑨CH3-CH═CH2⑩ ⑪
⑪ ⑫CH3Cl
⑫CH3Cl