题目内容
8.下列实验方法导致实验结果偏高的是( )| A. | 用标准盐酸滴定待测氢氧化钠溶液至终点,读数时视线偏高 | |
| B. | 用含Na2O的NaOH固体配制成的标准溶液,滴定待测盐酸 | |
| C. | 将4.0g NaOH溶解后迅速转移入1L的容量瓶中定容,配制0.1moL/L的NaOH溶液 | |
| D. | 将1mL 98%的浓硫酸加入9mL水中,配制9.8%的稀硫酸 |
分析 A.用标准盐酸滴定待测氢氧化钠溶液至终点,读数时视线偏高,导致盐酸体积偏小;
B.M(Na2O)>M(NaOH),二者质量相同时,n(Na2O)<n(NaOH),则用含Na2O的NaOH固体配制成的标准溶液c(NaOH)偏低;
C.NaOH溶解过程是放热过程,NaOH未冷却就转移溶液会导致平衡溶液体积偏小;
D.浓硫酸密度大于水密度,1mL98%的浓硫酸加入9mL水,浓硫酸质量大于1mL水的质量,导致配制溶液浓度大于9.8%.
解答 解:A.用标准盐酸滴定待测氢氧化钠溶液至终点,读数时视线偏高,导致盐酸体积偏小,则测定NaOH浓度偏低,故A错误;
B.M(Na2O)>M(NaOH),二者质量相同时,n(Na2O)<n(NaOH),则用含Na2O的NaOH固体配制成的标准溶液c(NaOH)偏低,用该溶液滴定盐酸时消耗V(NaOH)偏大,则测定盐酸浓度偏高,故B正确;
C.NaOH溶解过程是放热过程,NaOH未冷却就转移溶液会导致平衡溶液体积偏小,n(NaOH)不变,会导致c(NaOH)偏高,故C正确;
D.浓硫酸密度大于水密度,1mL98%的浓硫酸加入9mL水,浓硫酸质量大于1mL水的质量,导致配制溶液浓度大于9.8%,则配制溶液浓度偏高,故D正确;
故选BCD.
点评 本题考查化学实验评价,为高频考点,明确实验原理是解本题关键,会从实验基本操作方法、物质的性质方面来分析解答,注意滴定管中小刻度在上边、大刻度在下边,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下列表示对应的化学反应的离子方程式正确的是( )
| A. | FeO溶于稀硝酸:FeO+2H++NO3-=Fe3++NO↑+H2O | |
| B. | 氯化氢气体通入澄清石灰水中:HCl+OH-=H2O+Cl- | |
| C. | 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:2Ba2++OH-+H++2SO42-=2BaSO4↓+H2O | |
| D. | 在溶液中,氯化铝与烧碱按物质的量之比1:1混合:Al3++3OH-=Al(OH)3↓ |
19.化学是你,化学是我.下列有关说法错误的是( )
| A. | PVC保鲜膜属于链状聚合物,在加热时易熔化,能溶于氯仿 | |
| B. | 汽车尾气排放的NO2等气体是造成光化学污染的主要原因 | |
| C. | 焰色反应是金素元素的性质,属于化学变化 | |
| D. | 误食含有大量Cu2+的食物可以服用鲜牛奶解毒 |
16.下列说法中正确的是( )
| A. | 10 L 0.05mol•L-1Ba(OH)2溶液与10 L 0.05mol•L-1 H2SO4反应时的反应热是中和热 | |
| B. | 由2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ•mol-1知,该反应的反应热为571.6 kJ•mol-1 | |
| C. | 由2H2(l)+O2(l)=2H2O(g)△H=-482.6 kJ•mol-1知,H2的燃烧热为482.6 kJ•mol-1 | |
| D. | 由C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2221.5 kJ•mol-1知,气体C3H8的燃烧热为2221.5 kJ•mol-1 |
13.25℃时,在强碱性溶液中可以大量共存的离子组是( )
| A. | K+、Cu2+、SO32-、MnO4- | B. | NH4+、Fe2+、NO3-、H+ | ||
| C. | HCO3-、Na+、Mg2+、Cl- | D. | Na+、K+、SO42-、Cl- |
20.下列说法正确的是( )
| 元素 | 有关信息 |
| X | 所在主族序数与所在周期序数之差为4,在该周期中原子半径最小 |
| Y | 在最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
| Z | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
| W | 地壳中含量最高的金属元素 |
| A. | W与Y的最高价氧化物对应的水化物之间可相互反应 | |
| B. | 原子半径的大小顺序为:rX>rY>rW | |
| C. | 向浓ZX3溶液中滴加少量的Na2SO3溶液,可产生大量沉淀和气体 | |
| D. | 可用电解W与X形成的化合物来制取W单质 |
10.下列有关溶液配制的说法正确的是( )
| A. | 在50mL量筒中配制0.1000mol•L-1碳酸钠溶液 | |
| B. | 仅用烧杯、量筒、玻璃棒就可以配制100mL0.1000mol•L-1K2Cr2O7溶液 | |
| C. | 用100mL容量瓶、烧杯、玻璃棒、量筒、胶头滴管和pH=1的盐酸配制100mLpH=2的盐酸 | |
| D. | 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余液体吸出 |
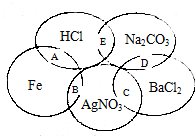 如图图为一五元环图案,小明在图案上依次写了五种物质,图中相交的两种物质均可发生化学反应,A、B、C、D、E表示其相应的化学反应.请回答下列问题:
如图图为一五元环图案,小明在图案上依次写了五种物质,图中相交的两种物质均可发生化学反应,A、B、C、D、E表示其相应的化学反应.请回答下列问题:
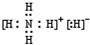 .
.