题目内容
18.小苏打片每片含0.42gNaHCO3,2片小苏打片和胃酸完全反应,消耗HCl的物质的量为( )| A. | 0.005mol | B. | 0.01mol | C. | 0.015mol | D. | 0.02mol |
分析 NaHCO3和稀盐酸反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,两片小苏打片中含有n(NaHCO3)=$\frac{0.42g}{84g/mol}×2$=0.01mol,根据碳酸氢钠与盐酸之间的关系式计算消耗盐酸的物质的量.
解答 解:NaHCO3和稀盐酸反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,两片小苏打片中含有n(NaHCO3)=$\frac{0.42g}{84g/mol}×2$=0.01mol,根据方程式知,n(NaHCO3)=n(HCl)=0.01mol,故选B.
点评 本题考查方程式的计算,为高频考点,侧重考查学生计算能力,正确书写方程式是解本题关键,注意知识的灵活运用,题目难度不大.

练习册系列答案
相关题目
8.Ⅰ.有硫酸酸化的草酸(H2C2O4,二元弱酸)溶液能将KMnO4溶液中的MnO4-转化为Mn2+.某化学小组研究发现,少量MnSO4可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,完成以下实验设计表.
(2)若t1<t2,则根据实验①和②得到的结论是溶液的pH对该反应的速率有影响.
(3)请你设计实验验证MnSO4对该反应起催化作用,完成下表中内容.
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,完成以下实验设计表.
| 实验 编号 | 温度 | 初始pH | 0.1 mol/L草酸溶液/mL | 0.01mol/LKMnO4溶液体积/mL | 蒸馏水体积/mL | 待测数据(反应混合液褪色时间/s) |
| ① | 常温 | 1 | 20 | 50 | 30 | t1 |
| ② | 常温 | 2 | 20 | 50 | 30 | t2 |
| ③ | 常温 | 2 | 40 | t3 |
(3)请你设计实验验证MnSO4对该反应起催化作用,完成下表中内容.
| 实验方案(不要求写出具体操作过程) | 预期实验结果和结论 |
| 往反应混合液中加入少量MnSO4固体,控制其他反应条件与实验①相同,进行对比实验 | 若反应混合液褪色时间小于实验①中的t1,则MnSO4对该反应起催化作用(若褪色时间相同,则MnSO4对该反应无催化作用) |
9.向一种溶液中滴加另一种溶液后,溶液的颜色不发生显著变化的是( )
| A. | 氯化亚铁溶液中加入双氧水 | |
| B. | 硫酸亚铁酸性溶液中滴加硝酸钾溶液 | |
| C. | 硫酸铜溶液中滴加硝酸钡溶液 | |
| D. | 高锰酸钾酸性溶液中滴加亚硫酸钠溶液 |
6.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 12 g C-13含有的原子数为NA个 | |
| B. | 46g NO2和46g N2O4含有的原子数均为3NA | |
| C. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| D. | 标准状况下,2.24L乙醇所含分子数为0.1 NA |
10.在相同的状况下有A、B两种气体,若VA=VB,质量WA=WB,则( )
| A. | MA=MB | B. | nA<nB | C. | nA>nB | D. | MA<MB |
17.化学反应C+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO中的还原剂是( )
| A. | C | B. | H2O | C. | H2 | D. | CO |

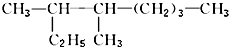 的名称3,4-二甲基辛烷.
的名称3,4-二甲基辛烷. .
.