题目内容
下列氧化还原反应方程式,所标电子转移方向与数目错误的是( )
A、 |
B、 |
C、 |
D、 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:A.该反应中Fe元素化合价由0价变为+2价、H元素化合价由+1价变为0价,得失电子的最小公倍数是2;
B.该反应中Cl元素化合价由+5价、-1价变为0价,得失电子总数是5;
C.该反应中Cl元素化合价由0价变为+1价、-1价,得失电子总数是2;
D.该反应中N元素化合价由+2价变为+5价、O元素化合价由0价变为-2价,得失电子总数是12.
B.该反应中Cl元素化合价由+5价、-1价变为0价,得失电子总数是5;
C.该反应中Cl元素化合价由0价变为+1价、-1价,得失电子总数是2;
D.该反应中N元素化合价由+2价变为+5价、O元素化合价由0价变为-2价,得失电子总数是12.
解答:
解:A.该反应中Fe元素化合价由0价变为+2价、H元素化合价由+1价变为0价,得失电子的最小公倍数是2, 中电子转移方向与数目正确,故A正确;
中电子转移方向与数目正确,故A正确;
B.该反应中Cl元素化合价由+5价、-1价变为0价,得失电子总数是5,其电子转移方向和数目为 ,故B错误;
,故B错误;
C.该反应中Cl元素化合价由0价变为+1价、-1价,得失电子总数是2,转移电子方向和数目为 ,故C正确;
,故C正确;
D.该反应中N元素化合价由+2价变为+5价、O元素化合价由0价变为-2价,得失电子总数是12,转移电子方向和数目为 ,故D正确;
,故D正确;
故选B.
 中电子转移方向与数目正确,故A正确;
中电子转移方向与数目正确,故A正确;B.该反应中Cl元素化合价由+5价、-1价变为0价,得失电子总数是5,其电子转移方向和数目为
 ,故B错误;
,故B错误;C.该反应中Cl元素化合价由0价变为+1价、-1价,得失电子总数是2,转移电子方向和数目为
 ,故C正确;
,故C正确;D.该反应中N元素化合价由+2价变为+5价、O元素化合价由0价变为-2价,得失电子总数是12,转移电子方向和数目为
 ,故D正确;
,故D正确;故选B.
点评:本题考查了电子转移方向和数目,根据元素化合价变化来分析解答,易错选项是B,该反应中部分HCl不参加氧化还原反应,为易错点.

练习册系列答案
相关题目
下面有关14C和14N的叙述正确的是( )
| A、14C与14N有相同的中子数 |
| B、C与C60互为同位素 |
| C、15N与14N互为同位素 |
| D、14C与14N是相同的核素 |
对可逆反应A(气)+2B(气)?2C(气)△H<0的平衡体系,下列说法错误的是( )
| A、使用催化剂,v正、v逆都改变,变化的倍数相同 |
| B、升高温度,v正、v逆都增大,v正增大的倍数小于v逆增大的倍数 |
| C、增大压强,v正、v逆反应的速率都增大,v正增大的倍数大于v逆增大的倍数 |
| D、降低温度,v正、v逆都减小,v正减小的倍数大于v逆减小的倍数 |
甲、乙两烧杯中各盛放有100mL 2mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,充分反应结束后测得生成的气体体积比为甲:乙=2:3,则加入铝粉的质量为( )
| A、5.4g | B、3.6g |
| C、2.7g | D、1.8g |
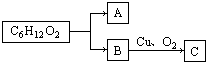 某酯的分子式为C6H12O2,其变化如图所示:若A能发生银镜反应,C不能发生银镜反应,则该酯的可能结构有( )
某酯的分子式为C6H12O2,其变化如图所示:若A能发生银镜反应,C不能发生银镜反应,则该酯的可能结构有( )| A、3种 | B、4种 | C、5种 | D、6种 |
下列各分子中所有原子未全部满足最外层为8个电子结构的是( )
| A、NH3 |
| B、PCl3 |
| C、CCl4 |
| D、CO2 |
按照无机物的分类方法,下列各组物质中,属于不同类型的物质是( )
| A、火碱、烧碱、生石灰 |
| B、生石灰、冰、干冰 |
| C、熟石灰、苛性钠、氢氧化钾 |
| D、纯碱、硫酸钠、胆矾 |
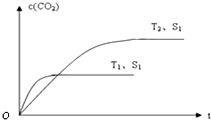 氮氧化物是空气的主要污染物,消除氮氧化物污染有多种方法.用催化技术可将超音速飞机尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO?2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下测得不同时间的NO和CO浓度如下表:
氮氧化物是空气的主要污染物,消除氮氧化物污染有多种方法.用催化技术可将超音速飞机尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO?2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下测得不同时间的NO和CO浓度如下表: