题目内容
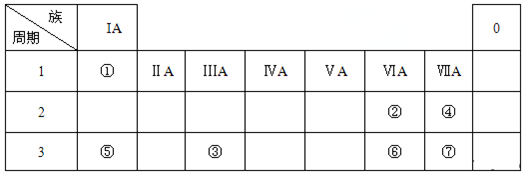
9.X、Y是短周期主族元素,常温常压下,两元素形成的单质分别为m、n,m为气态、n为固态,下列推断合理的是( )| A. | 若X,Y位于IA族,则化合物YX与水反应时水作还原剂 | |
| B. | 若X、Y位于第三周期,则X、Y形成的化合物只含离子键 | |
| C. | 若氢化物还原性HaX<HbY,则单质氧化性m>n | |
| D. | 若X、Y位于同一主族,则简单离子半径X>Y |
分析 X、Y是短周期主族元素,常温常压下,两元素形成的单质分别为m、n,m为气态、n为固态,
A.若X、Y位于IA族,X为H,Y为Na或Li;
B.若X、Y位于第三周期,Y为Cl,X为Na、Mg、Al、Si等;
C.若氢化物还原性HaX<HbY,可知非金属性X>Y;
D.若X、Y位于同一主族,如X为O,Y为S,电子层越多,离子半径越大.
解答 解:A.若X、Y位于IA族,X为H,Y为Na或Li,如NaH与水反应生成NaOH和氢气,水中H元素的化合价降低,水为氧化剂,故A错误;
B.若X、Y位于第三周期,Y为Cl,X为Na、Mg、Al、Si等,若形成氯化铝、四氯化硅,为共价化合物,故B错误;
C.若氢化物还原性HaX<HbY,可知非金属性X>Y,非金属性越强,对应单质氧化性越强,则单质氧化性m>n,故C正确;
D.若X、Y位于同一主族,如X为O,Y为S,电子层越多,离子半径越大,则简单离子半径X<Y,故D错误;
故选C.
点评 本题考查位置、结构与性质,为高频考点,把握元素在周期表的位置、元素化合物知识、元素周期律为解答的关键,侧重分析与应用能力的考查,注意结合实例分析,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
15.紫苏醇可抑制肿瘤发生,其结构简式如图,下列有关紫苏醇的叙述正确的是( )
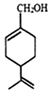

| A. | 分子式为C10H16O | |
| B. | 紫苏醇为芳香族化合物 | |
| C. | 环上的一氯取代物有四种 | |
| D. | 使酸性高锰酸钾溶液和溴水褪色的原理相同 |
17.已知:用Pt-Rh合金催化氧化NH3制NO,其反应的微观模型及含氮生成物产率随反应温度的变化曲线分别如图①、图②所示:下列说法中,不正确的是( )


| A. | 400℃时,生成的产物有N2、NO、H2O | |
| B. | 800℃时,反应的化学方程式是:4NH3+5O2$\frac{\underline{\;Pt-Rh\;}}{800℃}$ 4NO+6H2O | |
| C. | 400℃-800℃间,Pt-Rh合金对N2的吸附力逐渐减弱 | |
| D. | 800℃以上,发生了反应:2NO(g)?O2(g)+N2(g)△H>0 |
14.下列说法正确的是( )
| A. | 甲烷与氯气取代反应的产物二氯代甲烷无同分异构体说明甲烷是正四面体结构 | |
| B. | 等物质的量的乙烷与乙酸完全燃烧消耗氧气的量相等 | |
| C. | 按系统命名法,化合物 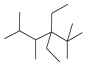 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 | |
| D. | 结构简式为 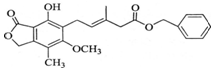 的化合物既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 的化合物既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 |
1.下列溶液中氢离子浓度最小的是( )
| A. | 10L0.10mol/LCH3COOH 溶液 | B. | 2L 0.05mol/L H2SO4溶液 | ||
| C. | lL0.10mol/LHNO3溶液 | D. | 2L0.1mol/LHCl溶液 |
18.下列物质的分子中既有σ键,又有π键的是( )
①CS2 ②H2O ③HCN ④H2O2 ⑤C2H4 ⑥HCHO.
①CS2 ②H2O ③HCN ④H2O2 ⑤C2H4 ⑥HCHO.
| A. | ①②③ | B. | ③④⑤⑥ | C. | ①③⑥ | D. | ①③⑤⑥ |
19.碱金属是典型的活泼金属,其根本原因是( )
| A. | 碱金属原子最外电子层上都只有1个电子,容易失去 | |
| B. | 碱金属在常温下易被氧化 | |
| C. | 碱金属单质的密度小,熔点和沸点低 | |
| D. | 碱金属原子的核电荷数比较小 |