题目内容
止咳酮(F)具有止咳、祛痰作用.其生产合成路线如下:

(1)已知烃A可以作为一个国家石油化工生产的标志,则A是 (填结构简式);由A合成B发生的化学反应类型有 (填字母).
a.加成反应 b.酯化反应 c.氧化反应 d.消去反应 e.加聚反应
(2)F中含有的官能团名称为
(3)C的核磁共振氢谱中可能出现 组吸收峰;
(4)已知D为氯代烃,C生成E为取代反应,写出C+D→E的化学方程式 .
(5)1mol F与1mol H2加成后生成有机物M,满足下列条件的M的同分异构体有 种.
①苯的二元取代物
②1mol M能与含2mol Br2的浓溴水完全发生反应
写出取代基无支链的一种结构
(6)目前我国用粮食发酵生产丙酮(CH3COCH3)占较大比重.利用题给相关信息,以淀粉为原料,合成丙酮的流程图如下.请将虚线处过程补充完整.合成过程中无机试剂任选.
(C6H10O5)n
C6H10O5
…
CHC3OCH3.

(1)已知烃A可以作为一个国家石油化工生产的标志,则A是
a.加成反应 b.酯化反应 c.氧化反应 d.消去反应 e.加聚反应
(2)F中含有的官能团名称为
(3)C的核磁共振氢谱中可能出现
(4)已知D为氯代烃,C生成E为取代反应,写出C+D→E的化学方程式
(5)1mol F与1mol H2加成后生成有机物M,满足下列条件的M的同分异构体有
①苯的二元取代物
②1mol M能与含2mol Br2的浓溴水完全发生反应
写出取代基无支链的一种结构
(6)目前我国用粮食发酵生产丙酮(CH3COCH3)占较大比重.利用题给相关信息,以淀粉为原料,合成丙酮的流程图如下.请将虚线处过程补充完整.合成过程中无机试剂任选.
(C6H10O5)n
| 酸或酶 |
| 酒化酶 |
| ①NaOH |
| ②H+△ |
考点:有机物的合成
专题:有机物的化学性质及推断
分析:(1)烃A可以作为一个国家石油化工生产的标志,则A为乙烯,乙烯与水发生加成反应生成乙醇,乙醇发生氧化反应生成乙酸,乙酸与乙醇发生酯化反应得到乙酸乙酯;
(2)由F的结构可知含氧官能团为羰基;
(3)有几种化学环境不同的氢原子,其核磁共振氢谱就有几组吸收峰;
(4)D为氯代烃,C生成E为取代反应,对比C、E的结构可知,C为 ,反应同时生成HCl;
,反应同时生成HCl;
(5)1mol F与1mol H2加成后生成有机物M为 ,满足下列条件的M的同分异构体;①苯的二元取代物,②1mol M能与含2mol Br2的浓溴水完全发生反应,含有酚羟基,另外取代基为丁基,与羟基处于邻位或对位,再根据丁基异构判断可能的同分异构体,若取代基无支链,则丁基为-CH2CH2CH2CH3;
,满足下列条件的M的同分异构体;①苯的二元取代物,②1mol M能与含2mol Br2的浓溴水完全发生反应,含有酚羟基,另外取代基为丁基,与羟基处于邻位或对位,再根据丁基异构判断可能的同分异构体,若取代基无支链,则丁基为-CH2CH2CH2CH3;
(6)利用转化关系中B→C及E→F的转化进行设计,葡萄糖再酒化酶作用下得到乙醇,乙醇氧化得到乙酸,乙酸与乙醇发生酯化反应生成乙酸乙酯,乙酸乙酯在Na的作用下得到CH3COCH2COOC2H5,最后再经过①氢氧化钠、②酸得到丙酮.
(2)由F的结构可知含氧官能团为羰基;
(3)有几种化学环境不同的氢原子,其核磁共振氢谱就有几组吸收峰;
(4)D为氯代烃,C生成E为取代反应,对比C、E的结构可知,C为
 ,反应同时生成HCl;
,反应同时生成HCl;(5)1mol F与1mol H2加成后生成有机物M为
 ,满足下列条件的M的同分异构体;①苯的二元取代物,②1mol M能与含2mol Br2的浓溴水完全发生反应,含有酚羟基,另外取代基为丁基,与羟基处于邻位或对位,再根据丁基异构判断可能的同分异构体,若取代基无支链,则丁基为-CH2CH2CH2CH3;
,满足下列条件的M的同分异构体;①苯的二元取代物,②1mol M能与含2mol Br2的浓溴水完全发生反应,含有酚羟基,另外取代基为丁基,与羟基处于邻位或对位,再根据丁基异构判断可能的同分异构体,若取代基无支链,则丁基为-CH2CH2CH2CH3;(6)利用转化关系中B→C及E→F的转化进行设计,葡萄糖再酒化酶作用下得到乙醇,乙醇氧化得到乙酸,乙酸与乙醇发生酯化反应生成乙酸乙酯,乙酸乙酯在Na的作用下得到CH3COCH2COOC2H5,最后再经过①氢氧化钠、②酸得到丙酮.
解答:
解:(1)烃A可以作为一个国家石油化工生产的标志,则A为乙烯,结构简式为:H2C=CH2,A合成B路线为:乙烯与水发生加成反应生成乙醇,乙醇发生氧化反应生成乙酸,乙酸与乙醇发生酯化反应得到乙酸乙酯,故答案为:H2C=CH2;abc;
(2)由F的结构可知含氧官能团为羰基,故答案为:羰基;
(3)C分子有4种化学环境不同的氢原子,其核磁共振氢谱就有4组吸收峰,故答案为:4;
(4)D为氯代烃,C生成E为取代反应,对比C、E的结构可知,C为 ,反应同时生成HCl,反应方程式为:
,反应同时生成HCl,反应方程式为: ,
,
故答案为: ;
;
(5)1mol F与1mol H2加成后生成有机物M为 ,满足下列条件的M的同分异构体;①苯的二元取代物,②1mol M能与含2mol Br2的浓溴水完全发生反应,含有酚羟基,另外取代基为丁基,与羟基处于邻位或对位,丁基有-CH2CH2CH2CH3、-CH(CH3)2CH2CH3、-CH2C(CH3)2、-C(CH3)3,故共有8种,若取代基无支链,则丁基为-CH2CH2CH2CH3,符合条件一种同分异构体为
,满足下列条件的M的同分异构体;①苯的二元取代物,②1mol M能与含2mol Br2的浓溴水完全发生反应,含有酚羟基,另外取代基为丁基,与羟基处于邻位或对位,丁基有-CH2CH2CH2CH3、-CH(CH3)2CH2CH3、-CH2C(CH3)2、-C(CH3)3,故共有8种,若取代基无支链,则丁基为-CH2CH2CH2CH3,符合条件一种同分异构体为 ,
,
故答案为:8; ;
;
(6)利用转化关系中B→C及E→F的转化进行设计,葡萄糖再酒化酶作用下得到乙醇,乙醇氧化得到乙酸,乙酸与乙醇发生酯化反应生成乙酸乙酯,乙酸乙酯在Na的作用下得到CH3COCH2COOC2H5,最后再经过①氢氧化钠、②酸得到丙酮,虚线处路线图为: ,
,
故答案为: .
.
(2)由F的结构可知含氧官能团为羰基,故答案为:羰基;
(3)C分子有4种化学环境不同的氢原子,其核磁共振氢谱就有4组吸收峰,故答案为:4;
(4)D为氯代烃,C生成E为取代反应,对比C、E的结构可知,C为
 ,反应同时生成HCl,反应方程式为:
,反应同时生成HCl,反应方程式为: ,
,故答案为:
 ;
;(5)1mol F与1mol H2加成后生成有机物M为
 ,满足下列条件的M的同分异构体;①苯的二元取代物,②1mol M能与含2mol Br2的浓溴水完全发生反应,含有酚羟基,另外取代基为丁基,与羟基处于邻位或对位,丁基有-CH2CH2CH2CH3、-CH(CH3)2CH2CH3、-CH2C(CH3)2、-C(CH3)3,故共有8种,若取代基无支链,则丁基为-CH2CH2CH2CH3,符合条件一种同分异构体为
,满足下列条件的M的同分异构体;①苯的二元取代物,②1mol M能与含2mol Br2的浓溴水完全发生反应,含有酚羟基,另外取代基为丁基,与羟基处于邻位或对位,丁基有-CH2CH2CH2CH3、-CH(CH3)2CH2CH3、-CH2C(CH3)2、-C(CH3)3,故共有8种,若取代基无支链,则丁基为-CH2CH2CH2CH3,符合条件一种同分异构体为 ,
,故答案为:8;
 ;
;(6)利用转化关系中B→C及E→F的转化进行设计,葡萄糖再酒化酶作用下得到乙醇,乙醇氧化得到乙酸,乙酸与乙醇发生酯化反应生成乙酸乙酯,乙酸乙酯在Na的作用下得到CH3COCH2COOC2H5,最后再经过①氢氧化钠、②酸得到丙酮,虚线处路线图为:
 ,
,故答案为:
 .
.
点评:本题考查有机物的推断与合成、有机反应类型、官能团结构、有机反应方程式书写、同分异构体书写等,水对学生综合能力的考查,充分利用有机物的结构判断发生的反应,需要学生熟练掌握官能团的性质与转化,(6)中合成路线设计需要学生对转化中的反应进行利用,较好的考查学生知识迁移运用能力,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
当光束通过下列分散系时,可能产生丁达尔效应的是( )
| A、NaHCO3溶液 |
| B、蔗糖溶液 |
| C、CuSO4溶液 |
| D、Fe(OH)3胶体 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、c(H+)<c(OH-)的溶液中,Na+、K+、SO42-、ClO- |
| B、能使酚酞变红的溶液中:Na+、Cu2+、CO32-、NO3- |
| C、0.1mol?L-1FeCl3溶液中:K+、NH4-、I-、SCN- |
| D、加入铝粉能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42- |
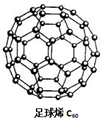 C60可用作储存氢气的材料,结构如图所示.继C60后,科学家又合成了Si60、N60,三种物质结构相似.下列有关说法正确的是( )
C60可用作储存氢气的材料,结构如图所示.继C60后,科学家又合成了Si60、N60,三种物质结构相似.下列有关说法正确的是( )| A、C60、Si60、N60都属于原子晶体 |
| B、C60、Si60、N60分子内共用电子对数目相同 |
| C、由于N-N键能小于N≡N,故N60的稳定性弱于N2 |
| D、由于C-C键长小于Si-Si键,所以C60熔沸点低于Si60 |

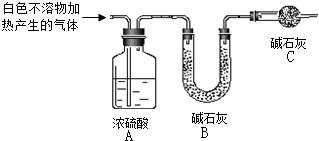 资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学通过如下实验探究反应原理并验证产物.
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学通过如下实验探究反应原理并验证产物.