题目内容
9.乙烯和丙烯按1:1(物质的量)聚合时,生成聚合乙丙树脂,该聚合物的结构是( )
| A. | ①② | B. | ②③ | C. | ①④ | D. | ①③ |
分析 凡含有不饱和键(双键、叁键、共轭双键)的化合物,在催化剂、引发剂或辐射等外加条件作用下,相互加成形成新的共价键相连大分子的反应就是加聚反应,可以是同物质之间加成聚合也可是不同物质间加成聚合;
CH2=CH2与CH3CH=CH2按物质的量之比1:1聚合时,生成高分子化合物的结构简式可能为: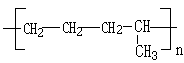
 .
.
解答 解:不饱和化合物发生加聚反应时,双键中的有一个键断裂,不饱和的碳原子相互连接成为长链,双键两侧碳原子上的原子团,不能在高聚物的主碳链上;CH2=CH2与CH3CH=CH2按物质的量之比1:1聚合时,发生反应的化学反应方程式有:
nCH2=CH2+nCH3CH=CH2$\stackrel{催化剂}{→}$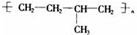 、nCH2=CH2+nCH3CH=CH2$\stackrel{催化剂}{→}$
、nCH2=CH2+nCH3CH=CH2$\stackrel{催化剂}{→}$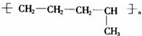 ,
,
所以该高聚物的结构简式为: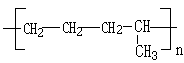
 ,
,
故选A.
点评 本题考查了同分异构体的书写、由单体判断高聚物的结构,题目难度不大,注意掌握加聚反应原理,明确根据高聚物判断单体的方法.

练习册系列答案
相关题目
20.下列有关元素非金属性的比较,正确的是( )
| A. | 进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱 | |
| B. | HCl溶液的酸性比H2S溶液的酸性强,则氯元素的非金属性比硫强 | |
| C. | H2O的沸点高于H2S,则氧元素的非金属性强于硫元素 | |
| D. | 浓H2SO4的氧化性强于HClO4,可确定硫和氯两种元素的非金属性强弱 |
17.已知有四种有机物A、B、C、D,其分子式均为C3H6O2,分子结构中均有甲基把它们分别进行实验并记录现象如下:
则A、B的结构简式为:ACH3CH2COOH;BCH3CHOHCHO;C、D的名称:C甲酸乙酯;D乙酸甲酯.
| 有机物 | 氢氧化钠 | 银氨溶液 | 新制氢氧化铜 | 金属钠 |
| A | 发生中和反应 | 不反应 | 溶解 | 放出氢气 |
| B | 不反应 | 发生银镜反应 | 生成红色沉淀 | 放出氢气 |
| C | 发生水解反应 | 发生银镜反应 | 生成红色沉淀 | 不反应 |
| D | 发生水解反应 | 不反应 | 不反应 | 不反应 |
4.下列对分子的性质的解释中,不正确的是( )
| A. | 水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致 | |
| B. | 乳酸( )有一对手性异构体,因为其分子中含有一个手性碳原子 )有一对手性异构体,因为其分子中含有一个手性碳原子 | |
| C. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| D. | 由图 知酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数大于次氯酸的非羟基氧原子数 知酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数大于次氯酸的非羟基氧原子数 |
1.下列说法不正确的是( )
| A. | 实验室少量的金属钠保存在煤油或石蜡油里 | |
| B. | 金属钠着火,用干燥的沙土来灭火 | |
| C. | 铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物 | |
| D. | 铁制炊具不宜用来煎炒食物,因为铁要与水反应 |
18.在一定温度下,反应:2A(s)+2B(g)?C(g)+D(g)在恒容的密闭容器中进行,能说明该反应已经达到平衡的是( )
| A. | 容器内的压强不随时间而变化 | |
| B. | B的正反应速率等于C的逆反应速率 | |
| C. | A的质量不再改变 | |
| D. | 单位时间内生成2a mol A,同时消耗a mol C |
19.一定温度下可逆反应N2(g)+3H2(g)?2NH3(g)达平衡的标准是:(分别用V(正)表示正反应速率,V(逆)表示逆反应速率)( )
| A. | 2V(正)(N2)=V(逆)(NH3) | B. | V(正)(N2)=3V(正)(H2) | ||
| C. | 2V(正)(H2)=3V(逆)(NH3) | D. | N2、H2、NH3的体积比为1:3:2 |
 与
与
 与
与
 与
与
 与
与
