题目内容
13.写出下列有机方程式:①丙烯聚合:

②甲苯的硝化反应:

③实验室制乙炔:CaC2+2H2O=Ca(OH)2+C2H2↑.
分析 ①丙烯分子中含有碳碳双键,在一定条件下能够发生加聚反应生成聚丙烯,据此写出该反应的化学方程式;
②甲苯与浓硝酸在浓硫酸做催化剂条件下生成2,4,6-三硝基甲苯;
③碳化钙与水反应生成氢氧化钙和乙炔.
解答 解:①聚丙烯分子中含有不饱和的碳碳双键,在一定条件下能够发生加聚反应得到聚丙烯,反应的化学方程式为: ,
,
故答案为: ;
;
②甲苯可以和浓硝酸之间发生取代反应生成2,4,6-三硝基甲苯,即TNT,化学反应方程式为: ,
,
故答案为: ;
;
③碳化钙与食盐水反应制备乙炔,该反应为CaC2+2H2O=Ca(OH)2+C2H2↑,
故答案为:CaC2+2H2O=Ca(OH)2+C2H2↑.
点评 本题考查有机化学反应方程式书写,为高频考点,把握有机物的结构与性质、官能团与性质的关系为解答的关键,注意有机反应类型及反应条件,题目难度不大.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
1.下列是我们日常生活中接触到的物质,其中属于纯净物的是( )
| A. | 蒸馏水 | B. | 可口可乐 | C. | 食醋 | D. | 洁净的空气 |
8.实验室欲配制480mL浓度为0.1mol•L-1的Na2CO3溶液,下列操作可以实现的是( )
| A. | 称量5.3 g Na2CO3固体溶于480 mL水配制成溶液 | |
| B. | 称量5.3 g Na2CO3固体溶于水配制成0.5 L溶液 | |
| C. | 称量5.3 g Na2CO3•10H2O晶体溶于水配制成0.5 L溶液 | |
| D. | 称量5.3 g Na2CO3•10H2O晶体溶于0.5 L水配制成溶液 |
18.反应X(g)+Y(g)?2Z(g)△H<0,达到平衡时,下列说法正确的是( )
| A. | 增大压强,平衡向右移动 | B. | 加入催化剂,Z的产率增大 | ||
| C. | 增大c(X),X的转化率增大 | D. | 降低温度,Y的转化率增大 |
5.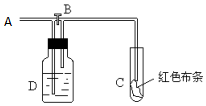 如图:A处通入氯气.打开B阀时,C处红色布条无变化,关闭B阀时,C处干燥的红色布条褪色.由此作出的判断正确的是( )
如图:A处通入氯气.打开B阀时,C处红色布条无变化,关闭B阀时,C处干燥的红色布条褪色.由此作出的判断正确的是( )
a.D中不可能是浓硫酸 b.D中可以是少量水
c.通入的氯气含有水蒸气 d.D中可以是饱和食盐水.
 如图:A处通入氯气.打开B阀时,C处红色布条无变化,关闭B阀时,C处干燥的红色布条褪色.由此作出的判断正确的是( )
如图:A处通入氯气.打开B阀时,C处红色布条无变化,关闭B阀时,C处干燥的红色布条褪色.由此作出的判断正确的是( )a.D中不可能是浓硫酸 b.D中可以是少量水
c.通入的氯气含有水蒸气 d.D中可以是饱和食盐水.
| A. | abc | B. | bcd | C. | abd | D. | abcd |
17.在一定温度下,容器内M、N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是( )
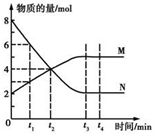

| A. | 反应的化学方程式为2 M?N | |
| B. | t2 min时,正逆反应速率相等,反应达到平衡 | |
| C. | t3 min后,正逆反应仍在进行 | |
| D. | t3~t4 min时,v正(N)=v逆(M) |
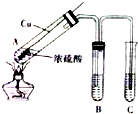 浓硫酸是一种重要的化工产品.
浓硫酸是一种重要的化工产品.