题目内容
4.与22g CO2所含氧原子数相等的物质是( )| A. | 标况下11.2LNO2分子 | B. | 0.3mol H2SO4分子 | ||
| C. | 1L 0.5mol/LBa(OH)2溶液 | D. | 12.04×1023个SO3分子 |
分析 22g CO2 n(CO2)=$\frac{22g}{44g/mol}$=0.5mol,每个分子中含有2个O原子,则n(O)=2n(CO2)=2×0.5mol=1mol,根据N=nNA知,氧原子个数相等,说明O原子物质的量相等,据此分析解答.
解答 解:22g CO2 n(CO2)=$\frac{22g}{44g/mol}$=0.5mol,每个分子中含有2个O原子,则n(O)=2n(CO2)=2×0.5mol=1mol,根据N=nNA知,氧原子个数相等,说明O原子物质的量相等为1mol,
A.标况下11.2LNO2中n(NO2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,每个二氧化氮分子中含有两个O原子,所以氧原子物质的量为1mol,故A正确;
B.0.3mol H2SO4分子中氧原子物质的量=0.3mol×4=1.2mol,故B错误;
C.1L 0.5mol/L Ba(OH)2中n(O)=2n[Ba(OH)2]=2×0.5mol/L×1L=1mol,但溶液中还含有水,所以总的O原子物质的量远远大于1mol,故C错误;
D.12.04×1023个SO3分子物质的量=$\frac{12.04×1{0}^{23}}{6.02×1{0}^{23}/mol}$=2mol,每个分子中含有3个O原子,所以O原子总物质的量6mol,故D错误;
故选A.
点评 本题考查物质的量有关计算,为高频考点,明确各个物理量之间的关系是解本题关键,侧重考查学生分析能使能力,易错选项是C,易漏掉水中的O原子而导致错误.

练习册系列答案
相关题目
14.下列有关元素周期律的叙述中,正确的是( )
| A. | 非金属性强弱:F2<Cl2 | B. | 金属性强弱:K<Na | ||
| C. | 酸性强弱:H2SO4<HClO4 | D. | 碱性强弱:NaOH<Mg(OH)2 |
15.下列说法错误的是( )
| A. | 同浓度的下列溶液,c(NH4+)大小顺序:(NH4)2SO4>NH4HSO4>NH4Cl>NH4HCO3 | |
| B. | 同浓度的下列溶液,pH值大小顺序:Na2CO3>NaClO>NaHCO3>CH3COONa | |
| C. | 用水冲洗BaSO4比用稀硫酸冲洗损失大 | |
| D. | 用惰性电极电解某溶液,两极分别产生H2和O2,pH值一定升高 |
12.下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1mol/L NaHCO3溶液,c(Na+)>c(OH-)>c(HCO3-)>c(H+) | |
| B. | 0.1mol/L K2S溶液中,c(K+)=c(S2-)+c(HS-)+c(H2S) | |
| C. | 常温时pH=2的盐酸和pH=12的氨水中由水电离出的c(H+)相等 | |
| D. | pH=3的盐酸和pH=11的氨水等体积混合完全反应后c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
19.下列有关SO2说法中不正确的是( )
| A. | SO2是污染大气的有害气体之一 | |
| B. | SO2在大气中与水反应生成硫酸,产生酸雨 | |
| C. | SO2可使澄清石灰水变浑浊 | |
| D. | SO2能使品红溶液褪色,加热溶液颜色恢复 |
16.对下列装置图的叙述正确的是( )


| A. | 装置①可用于加热蒸干氯化铵溶液得到氯化铵晶体 | |
| B. | 装置②可用于铜和稀硝酸制取并收集少量NO | |
| C. | 装置③可用于证明铁生锈氧气参与反应 | |
| D. | 苯萃取碘水中的碘后,从装置④下口放出的是碘的苯溶液 |
13.下列废弃物,不可能直接回收利用的是( )
| A. | 易拉罐 | B. | 塑料拖鞋 | C. | 玻璃白酒瓶 | D. | 医用点滴管 |
14.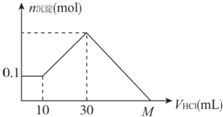 某一固体物质可能由NaOH、AlCl3、MgCl2中的几种组成,将其一定量溶于水,有沉淀产生,在所得悬浊液中逐滴加入5 mol/L的盐酸,图表示盐酸加入量与沉淀量的变化关系,图中M点表示已加入的盐酸体积,则M点的体积是( )
某一固体物质可能由NaOH、AlCl3、MgCl2中的几种组成,将其一定量溶于水,有沉淀产生,在所得悬浊液中逐滴加入5 mol/L的盐酸,图表示盐酸加入量与沉淀量的变化关系,图中M点表示已加入的盐酸体积,则M点的体积是( )
 某一固体物质可能由NaOH、AlCl3、MgCl2中的几种组成,将其一定量溶于水,有沉淀产生,在所得悬浊液中逐滴加入5 mol/L的盐酸,图表示盐酸加入量与沉淀量的变化关系,图中M点表示已加入的盐酸体积,则M点的体积是( )
某一固体物质可能由NaOH、AlCl3、MgCl2中的几种组成,将其一定量溶于水,有沉淀产生,在所得悬浊液中逐滴加入5 mol/L的盐酸,图表示盐酸加入量与沉淀量的变化关系,图中M点表示已加入的盐酸体积,则M点的体积是( )| A. | 70 mL | B. | 90 mL | C. | 100 mL | D. | 130 mL |