题目内容
12.下列溶液中微粒的物质的量浓度关系正确的是( )| A. | 0.1mol/L NaHCO3溶液,c(Na+)>c(OH-)>c(HCO3-)>c(H+) | |
| B. | 0.1mol/L K2S溶液中,c(K+)=c(S2-)+c(HS-)+c(H2S) | |
| C. | 常温时pH=2的盐酸和pH=12的氨水中由水电离出的c(H+)相等 | |
| D. | pH=3的盐酸和pH=11的氨水等体积混合完全反应后c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
分析 A.常温下,0.1mol•L-1NaHCO3溶液中HCO3-水解程度大于电离程度导致溶液呈碱性,但其水解和电离程度都较小,水还电离生成OH-,Na+不水解,据此判断离子浓度大小;
B.溶液中存在物料守恒,n(K)=2n(S);
C.常温时pH=2的盐酸溶液中氢离子浓度和pH=12的氨水中氢氧根离子浓度相同,对水的电离抑制程度相同;
D.pH=3的盐酸和pH=11的氨水等体积混合完全反应氨水溶液中一水合氨又电离出氢氧根离子,溶液显碱性,铵根离子浓度大于氯离子浓度.
解答 解:A.1mol•L-1NaHCO3溶液中HCO3-水解程度大于电离程度导致溶液呈碱性,但其水解和电离程度都较小,水还电离生成OH-,Na+不水解,则离子浓度大小顺序是c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-),故A错误;
B.0.1mol/L K2S溶液中存在物料守恒,c(K+)=2c(S2-)+2c(HS-)+2c(H2S),故C错误;
C.常温时pH=2的盐酸溶液中氢离子浓度和pH=12的氨水中氢氧根离子浓度相同,对水的电离抑制程度相同,由水电离出的c(H+)相等为10-2mol/L,故C正确;
D.pH=3的盐酸和pH=11的氨水等体积混合完全反应氨水溶液中一水合氨又电离出氢氧根离子,溶液显碱性,铵根离子浓度大于氯离子浓度,溶液中离子浓度大小为:c(NH4+)>c(Cl-)>c(OH-)>c(H+),故D错误;
故选C.
点评 本题考查了电解质溶液中离子浓度大小、电解质溶液中电荷守恒、物料守恒、弱电解质电离平衡影响因素等知识,题目难度中等.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
3.对有关NaClO和NaCl混合溶液的叙述正确的是( )
| A. | 该溶液中,H+、NH4+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,K+、OH-、S2-、NO3-能大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,离子方程式为:2Fe2++ClO-+2H+→Cl-+2Fe3++H2O | |
| D. | 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
7.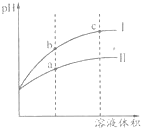 某温度下pH=2的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如图所示.下列说法正确的是( )
某温度下pH=2的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如图所示.下列说法正确的是( )
 某温度下pH=2的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如图所示.下列说法正确的是( )
某温度下pH=2的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如图所示.下列说法正确的是( )| A. | Ⅱ为盐酸稀释时pH变化曲线 | |
| B. | b点溶液的导电性比c点溶液的导电性强 | |
| C. | a点Kw数值比c点Kw数值大 | |
| D. | pH=2的盐酸和醋酸,盐酸的物质的量浓度大 |
17.生活或实验中常碰到一些化学知识,下列分析中不正确的是( )
| A. | 人体不能缺碘,需要正常补碘.“加碘食盐”中的“碘”是指碘元素 | |
| B. | 进行焰色反应实验时,蘸取样品之前需要用稀硫酸溶液清洗铂丝 | |
| C. | “绿色化学”的理想在于不再使用有毒、有害的物质,不再产生废物 | |
| D. | 水壶中产生的水垢可用食醋清洗除去 |
4.与22g CO2所含氧原子数相等的物质是( )
| A. | 标况下11.2LNO2分子 | B. | 0.3mol H2SO4分子 | ||
| C. | 1L 0.5mol/LBa(OH)2溶液 | D. | 12.04×1023个SO3分子 |
1.下列有机化学反应属于水解反应的是( )
| A. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| B. | 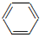 +HO-Na2$→_{60℃}^{浓硫酸}$ +HO-Na2$→_{60℃}^{浓硫酸}$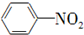 +H2O +H2O | |
| C. | CH2═CH2+H2O$\stackrel{催化剂}{→}$CH3-CH2OH | |
| D. | CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH |
2.25℃、101kPa下:①2Na(s)+$\frac{1}{2}$O2(g)=Na2O(s)△H=-414kJ.mol-1
②2Na(s)+O2(g)=Na2O2(s)△H=-511kJ.mol-1
下列说法不正确的是( )
②2Na(s)+O2(g)=Na2O2(s)△H=-511kJ.mol-1
下列说法不正确的是( )
| A. | ①和②产物的阴阳离子个数比相等 | |
| B. | ①和②生成等物质的量的产物,转移电子数相同 | |
| C. | 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 | |
| D. | 25℃、101kPa下:Na2O2(s)+2Na(s)=2Na2O(s)△H=-317kJ.mol-1 |
 ;
; CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.