题目内容
 将20mL 0.10mol?L-1CH3COOH溶液和20mL 0.10mol?L-1的HSCN溶液分别与0.10mol?L-1的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与时间t的关系如图所示.
将20mL 0.10mol?L-1CH3COOH溶液和20mL 0.10mol?L-1的HSCN溶液分别与0.10mol?L-1的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与时间t的关系如图所示.反应开始时,两种溶液产生CO2的速率明显不同的原因是
考点:弱电解质在水溶液中的电离平衡
专题:
分析:由生成二氧化碳的曲线斜率可知HSCN反应较快,则可知HSCN中中c(H+)较大,说明HSCN酸性较强,再利用盐类水解的规律来分析离子浓度的关系.
解答:
解:由Ka(CH3COOH)=1.8×10-5和Ka(HSCN)=0.13可知,CH3COOH的酸性弱于HSCN的,即在相同浓度的情况下HSCN溶液中H+的浓度大于CH3COOH溶液中H+的浓度,浓度越大反应速率越快;又酸越弱,反应生成的相应的钠盐越易水解,即c(CH3COO-)<c(SCN-),
故答案为:HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快;<.
故答案为:HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快;<.
点评:本题考查弱电解质的电离、盐类水解的关系,为高频考点,题目以图象题的形式较好的训练学生利用信息来分析问题、解决问题的能力,注意把握题目的分析,难度不大.

练习册系列答案
相关题目
2014年“世界水日”和“世界水周”的活动主题为“加强合乎管理,建设生态文明”下列关于水的说法正确的是( )
| A、为了保护水资源,禁止使用化肥 |
| B、用电解大量水的方法获得清洁能源氧气 |
| C、4℃时,纯水的pH=7 |
| D、城市浇花,采用喷灌、滴滴灌技术 |
下列叙述正确的是( )
| A、氯气的水溶液可以导电,氯气是电解质 |
| B、在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+ )增大 |
| C、升高温度,可逆反应的化学平衡常数一定增大 |
| D、在 CH3COONa 溶液中加入适量 CH3COOH,可使 c( Na+)=c(CH3COO-) |
下列醇中既能发生消去反应,又能被氧化为酮的是( )
①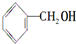 ②
② ③CH3OH④
③CH3OH④ ⑤
⑤ ⑥
⑥
①
 ②
② ③CH3OH④
③CH3OH④ ⑤
⑤ ⑥
⑥
| A、①④⑤ | B、②④⑥ |
| C、②⑥ | D、①②⑥ |
 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A在一定条件下可发生如图所示的转化,请回答下列问题:
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A在一定条件下可发生如图所示的转化,请回答下列问题: 某化学兴趣小组用100mL 1mol/L NaOH溶液完全吸收了a mol CO2后得到溶液A(液体体积无变化).为了确定溶液A的溶质成分及a值,该兴趣小组的同学进行了如下实验.请帮助他们完成下列相应实验内容.
某化学兴趣小组用100mL 1mol/L NaOH溶液完全吸收了a mol CO2后得到溶液A(液体体积无变化).为了确定溶液A的溶质成分及a值,该兴趣小组的同学进行了如下实验.请帮助他们完成下列相应实验内容.
