题目内容
化学与社会、生活密切相关.对下列现象或事实解释错误的是( )
| 选项 | 现象或事实 | 解释 |
| A | 明矾用于净水 | 铝离子水解产生的胶体具有很强吸附杂质的作用 |
| B | SO2能使溴水溶液褪色 | SO2具有还原性 |
| C | “地沟油”禁止食用,但可以用来制造肥皂 | “地沟油”主要成分为油脂属于酯类可以发生皂化反应 |
| D | 用氯水和淀粉溶液鉴别食盐是否加碘 | 目前加碘食盐中含碘元素物质为KI |
| A、A | B、B | C、C | D、D |
考点:胶体的应用,二氧化硫的化学性质,油脂的性质、组成与结构,常见的食品添加剂的组成、性质和作用
专题:
分析:A、根据明矾的净水原理来分析;
B、SO2有很强的还原性;
C、地沟油属于酯类;
D、KI有强还原性,易被氧化.
B、SO2有很强的还原性;
C、地沟油属于酯类;
D、KI有强还原性,易被氧化.
解答:
解:A、明矾能净水是由于电离出的Al3+能水解为Al(OH)3胶体,Al(OH)3胶体能吸附水中的杂质,起到净水的作用,故A正确;
B、SO2有很强的还原性,与溴水发生氧化还原反应:SO2+Br2+2H2O=2HCl+H2SO4,使溴水褪色,故B正确;
C、地沟油含有大量细菌和重金属,对人体健康有害,属于酯类物质,但可作为工业原料用于制取肥皂、汽油、柴油等,故C正确;
D、KI有强还原性,易被氧化,故加碘盐中加的不是KI,而是KIO3,故D错误.
故选D.
B、SO2有很强的还原性,与溴水发生氧化还原反应:SO2+Br2+2H2O=2HCl+H2SO4,使溴水褪色,故B正确;
C、地沟油含有大量细菌和重金属,对人体健康有害,属于酯类物质,但可作为工业原料用于制取肥皂、汽油、柴油等,故C正确;
D、KI有强还原性,易被氧化,故加碘盐中加的不是KI,而是KIO3,故D错误.
故选D.
点评:本题考查了常见的化学知识在生活中的应用,应注意的是明矾只能净水,不能消毒,难度不大.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
汽车尾气中含有NO2、NO和CO等有害气体,现取标准状况下22.4 L汽车尾气,研究发现该气体通过催化转化器后,上述三种有害气体可被完全转化为无害的N2和CO2,再取等体积尾气通入0.1 mol/L 50 mLNaOH溶液中,其中的NO2和NO恰好被完全吸收.则尾气中CO的体积分数可能为(说明:汽车尾气中其它成分气体与CO和NaOH溶液均不反应)( )
| A、0.4% | B、0.8% |
| C、2% | D、4% |
某同学通过系列实验探究铝及其化合物的性质,操作正确且能达到目的是( )
| A、将浓氨水缓慢滴入Al2(SO4)3溶液时候,观察Al(OH)3沉淀的生成和溶解 |
| B、将Al(OH)3浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
| C、将Al(OH)3沉淀转入蒸发皿中,加热至无水蒸气逸出,得氧化铝固体 |
| D、分别向Al(OH)3沉淀中加入稀硫酸和NaOH溶液,探究Al(OH)3的两性 |
同主族元素形成的同一类型化合物,往往其结构和性质相似.PH4I是一种白色晶体,下列对PH4I的叙述中,正确的是( )
| A、它是一种共价化合物 |
| B、它受热时,可能会分解产生有色气体 |
| C、它不可能与NaOH溶液反应 |
| D、它只含离子键 |


 为原料制取
为原料制取 ,是化工生产环已酮的基本原理,根据下列合成路线如下空:
,是化工生产环已酮的基本原理,根据下列合成路线如下空: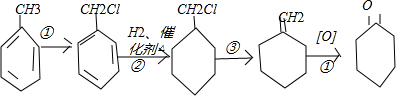
 将20mL 0.10mol?L-1CH3COOH溶液和20mL 0.10mol?L-1的HSCN溶液分别与0.10mol?L-1的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与时间t的关系如图所示.
将20mL 0.10mol?L-1CH3COOH溶液和20mL 0.10mol?L-1的HSCN溶液分别与0.10mol?L-1的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与时间t的关系如图所示.