题目内容
8.常温下把铝粉加入下列物质中,能产生氢气的是( )| A. | 硫酸钠溶液 | B. | 稀硝酸 | C. | 浓硫酸 | D. | 氯化铵溶液 |
分析 浓硫酸、硝酸具有强氧化性,与金属反应不生成氢气,以此来解答.
解答 解:A、硫酸钠溶液与铝不反应,故A错误;
B、稀硝酸强氧化性生成一氧化氮,故B错误;
C、浓硫酸发生钝化,故C错误;
D、氯化铵水解呈酸性,铝与水解产生的氢离子反应,促进水解,产生氢气的同时又有氨气放出,故D正确;
故选D.
点评 本题考查酸与铝的性质,明确硝酸、浓硫酸的强氧化性是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
19.分子式为C5H10O2,属于酯类的同分异构体有多少种( )
| A. | 9种 | B. | 13种 | C. | 10种 | D. | 11种 |
16.下列溶液中NO3-的物质的量浓度最大的是( )
| A. | 500 mL 1 mol•L-1的KNO3溶液 | |
| B. | 500 mL 1 mol•L-1的Ba(NO3)2溶液 | |
| C. | 1000 mL 0.5 mol•L-1的Mg(NO3)2溶液 | |
| D. | 1000 mL 0.5 mol•L-1的Fe(NO3)3溶液 |
3.下列通式只表示一类物质的是( )
| A. | CnH2n+2 | B. | CnH2n | C. | CnH2n-2 | D. | CnH2n-1Br |
13.下列说法正确的是( )
| A. | 绿色食品就是指颜色为绿色的食品 | B. | 有机食品是指含有机物的食品 | ||
| C. | OTC表示处方药 | D. | 加碘盐是在食盐中加入KIO3 |
20.下列过程中,有电能转化为化学能的是( )
| A. | 打手机 | B. | 光合作用 | C. | 电解水 | D. | 点燃氢气 |
18.下列说法中正确的是( )
| A. | 二次电池在充电时,电池的负极要与外接电源的负极相连 | |
| B. | 用惰性电极电解硫酸铜溶液一段时间后,加入氢氧化铜可恢复原状 | |
| C. | 化学腐蚀是生活中最常见的一种金属腐蚀 | |
| D. | 燃料电池中的电极材料必须活性不同 |
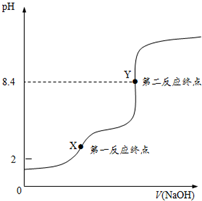 H2C2O4•2H2O(草酸,二元弱酸)和邻苯二甲酸氢钾均可作为标定NaOH溶液浓度的基准物质,从而获得NaOH标准溶液.
H2C2O4•2H2O(草酸,二元弱酸)和邻苯二甲酸氢钾均可作为标定NaOH溶液浓度的基准物质,从而获得NaOH标准溶液.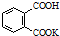 ,摩尔质量为204g•mol-1,易溶于水的固
,摩尔质量为204g•mol-1,易溶于水的固 化学在能源开发与利用中起着十分重要的作用.
化学在能源开发与利用中起着十分重要的作用.