题目内容
20.下列过程中,有电能转化为化学能的是( )| A. | 打手机 | B. | 光合作用 | C. | 电解水 | D. | 点燃氢气 |
分析 根据物质在发生化学反应时产生的能量转换方式来分析解答,
A.打手机是原电池反应转化为电能;
B.光合作用是吸收二氧化碳发生化学反应转化为葡萄糖;
C.电解水是通电后发生的氧化还原反应;
D.点燃氢气是气体氢气燃烧生成水;
解答 解:A、打手机是化学能转变为电能,故A错误.
B、光合作用是将光能转化为化学能,故B错误.
C、手机电池充电是将电能转化为化学能,故C正确.
D、点燃氢气是将化学能转变为热能和光能,故D错误.
故选C.
点评 本题考查了能量的转换,难度不大,根据物质在发生化学反应时能量的变化方式来分析解答即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.常温下把铝粉加入下列物质中,能产生氢气的是( )
| A. | 硫酸钠溶液 | B. | 稀硝酸 | C. | 浓硫酸 | D. | 氯化铵溶液 |
12.某学习小组在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.为了进一步研究硫酸铜的量对氢气生成速率的影响,该小组同学开始了实验探究.
(1)实验方案:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的锥形瓶中,收集产生的气体.记录单位时间氢气产生的体积.
其中:V1=30,V6=10,V9=17.5;
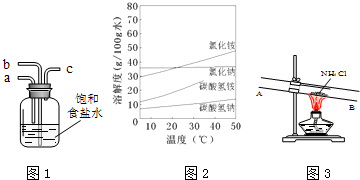
(2)实验装置:甲同学拟选用图1实验装置完成实验:

①你认为最简易的装置其连接顺序是:A接E接D接G(填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸就不能顺利滴入锥形瓶.请你帮助分析原因锌与稀硫酸反应放热且生成气体,使锥形瓶中气体压强变大.
③实验最后,在读取测量实验中生成氢气的总体积时,你认为合理的是ACD.
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
④乙同学认为可选用图2装置中的B(填A或B)直接与锥形瓶的导管A相连用以测量氢气的体积,理由是防止气体冷却时发生倒吸现象;实验结束时量筒内的液面高于水槽中液面,立即读数会使氢气的总体积偏大(填“偏大”“偏小”或“不变”);应进行的操作是应慢慢把量筒往下移,使量筒中液面恰好与水槽中液面相平;
(3)实验现象与结论:反应一段时间后,实验A中的金属呈灰黑色,实验E中的金属呈暗红色;该学习小组最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入一定量的硫酸铜后,生成的单质铜会沉积在锌的表面,降低了锌与溶液的接触面积.
(4)问题讨论:实验室中现有Na2SO4、MgSO4、AgSO4、K2SO4等4种溶液,可与实验中CuSO4溶液起相似作用的是Ag2SO4;要加快上述实验中气体产生的速率,还可采取的措施有升高反应温度;适当增加硫酸的浓度(答两种).
(1)实验方案:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的锥形瓶中,收集产生的气体.记录单位时间氢气产生的体积.
| 实验混合溶液 | A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
(2)实验装置:甲同学拟选用图1实验装置完成实验:

①你认为最简易的装置其连接顺序是:A接E接D接G(填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸就不能顺利滴入锥形瓶.请你帮助分析原因锌与稀硫酸反应放热且生成气体,使锥形瓶中气体压强变大.
③实验最后,在读取测量实验中生成氢气的总体积时,你认为合理的是ACD.
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
④乙同学认为可选用图2装置中的B(填A或B)直接与锥形瓶的导管A相连用以测量氢气的体积,理由是防止气体冷却时发生倒吸现象;实验结束时量筒内的液面高于水槽中液面,立即读数会使氢气的总体积偏大(填“偏大”“偏小”或“不变”);应进行的操作是应慢慢把量筒往下移,使量筒中液面恰好与水槽中液面相平;
(3)实验现象与结论:反应一段时间后,实验A中的金属呈灰黑色,实验E中的金属呈暗红色;该学习小组最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入一定量的硫酸铜后,生成的单质铜会沉积在锌的表面,降低了锌与溶液的接触面积.
(4)问题讨论:实验室中现有Na2SO4、MgSO4、AgSO4、K2SO4等4种溶液,可与实验中CuSO4溶液起相似作用的是Ag2SO4;要加快上述实验中气体产生的速率,还可采取的措施有升高反应温度;适当增加硫酸的浓度(答两种).
10.在100mL浓度为18mol/L、密度为ρg/mL的浓硫酸中,加入一定量的水,稀释成9mol/L的硫酸,则加入水的体积为( )
| A. | 小于100mL | B. | 等于100mL | C. | 大于100mL | D. | 等于$\frac{100}{ρ}$mL |

 .
.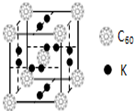 C60以其完美的球形结构受到科学家的高度重视,从此掀起了球形分子的研究热潮.继C60后,科学家又合成了Si60、N60等球形分子.
C60以其完美的球形结构受到科学家的高度重视,从此掀起了球形分子的研究热潮.继C60后,科学家又合成了Si60、N60等球形分子.