题目内容
2.现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相,甲、乙两元素相比较,金属性较强的是镁(填名称),可以验证该结论的实验是BC.A、将在空气中放置已久的这两种元素的块状单质分别放入热水中
B、将这两种元素的单质粉末分别和同浓度的盐酸反应
C、将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D、比较这两种元素的气态氢化物的稳定性.
分析 甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,则甲为Al,乙元素原子核外M电子层与K电子层上的电子数相等,则乙为Mg;
同周期自左而右元素金属性减弱,可以根据金属与水的反应难易、剧烈程度或金属和酸反应置换出氢气的难易或是最高价氧化物对应水化物的碱性强弱或金属单质之间的置换反应等来判断.
解答 解:甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,则甲为Al,乙元素原子核外M电子层与K电子层上的电子数相等,则乙为Mg,同周期自左而右元素金属性减弱,故金属性Mg>Al;
A.金属在在空气中放置已久,表面生成氧化物保护膜,阻止金属与水反应,不能比较金属性强弱,故A错误;
B.将除掉表面氧化膜的这两种元素的单质分别和同浓度的盐酸反应,反应越剧烈,则元素金属性越强,故B正确;
C.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液,比较碱性强弱,加入Mg粉的溶液呈浅红色,而加入Al粉的无明显现象,故C正确;
D.二者都是金属元素,不能比较氢化物的稳定性判断金属性强弱,故D错误,
故答案为:镁;BC.
点评 本题考查元素周期表与元素周期律,难度不大,从元素的结构和性质推断出元素种类是关键,注意掌握金属性、非金属性强弱比较与实验事实.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
10.2016年1月1日起,我国已开始施行修订后的《中华人民共和国大气污染防治法》.下列说法错误的是( )
| A. | 开发新能源,减少对化石能源的依赖 | |
| B. | 将燃煤进行脱硫处理,可减少酸雨的形成 | |
| C. | 雾霾(颗粒直径为2.5 x103 nm)具有丁达尔效应 | |
| D. | 推广使用电动汽车,可减少城市雾霾的形成 |
7.某元素的原子序数是34,则该基态原子中电子占据的原子轨道总数为( )
| A. | 17 | B. | 18 | C. | 19 | D. | 20 |
14.燃料电池是燃料(例如CO、H2、CH4等)跟氧气或空气起反应,将此反应的化学能转变为电能的装置,电解质溶液通常是KOH溶液.下列关于甲烷燃料电池的说法错误的是( )
| A. | 负极反应式为CH4+10OH--8e-═CO32-+7H2O | |
| B. | 正极反应式为O2+2H2O+4e-═4OH- | |
| C. | 随着不断放电,电解质溶液碱性不变 | |
| D. | 甲烷燃料电池也可以用稀硫酸做电解质溶液 |
12.具有下列电子层结构的原子或离子,其对应的元素一定属于同一周期的是( )
| A. | 两原子N层上都有1个s电子,一个原子无d电子,另一个原子有d电子 | |
| B. | 两原子其核外全部都是s电子 | |
| C. | 最外层电子排布为2s22p5的原子和最外层电子排布为2s22p6的离子 | |
| D. | 原子核外M层上的s、p能级都充满电子,而d能级上没有电子的两种原子 |

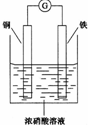 HN03和 HN02是氮的两种重要含氧酸.HN02能被常见的氧化剂(如高锰酸钾、重铬酸钾等)氧化;在酸性条件下也能被亚铁离子、碘离子还原;亚硝酸银( AgN02 )是一种难溶于水、易溶于酸的化合物.回答下列问题:
HN03和 HN02是氮的两种重要含氧酸.HN02能被常见的氧化剂(如高锰酸钾、重铬酸钾等)氧化;在酸性条件下也能被亚铁离子、碘离子还原;亚硝酸银( AgN02 )是一种难溶于水、易溶于酸的化合物.回答下列问题: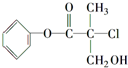 某有机物A是农药生产中的一种中间体,其结构简式如图所示.
某有机物A是农药生产中的一种中间体,其结构简式如图所示.