题目内容
常温下,下列离子浓度的关系正确的是
A.pH=2的盐酸与pH=12的氨水等体积混合:c(NH4+)=c(Cl-)>c(H+)=c(OH-)
B.0.2 mol·L-1的CH3COONa溶液与0.1 mol·L-1的HCl等体积混合:c(Na+)>c(Cl-)>c(CH3COO-)>c(H+)>c(OH-)
C.0.1 mol·L-1的HCN(弱酸)和0.1 mol·L-1的NaCN等体积混合:c(HCN)+c(CN-)+c(OH-)=c(Na+)+c(H+)
D.相同物质的量浓度时,溶液中c(NH4+)由大到小的顺序:NH4Al(SO4)2>NH4Cl>CH3COONH4>NH3·H2O
D
【解析】
试题分析:A.pH=2的盐酸与pH=12的氨水,氨水浓度大于HCl,二者等体积混合,氨水剩余,溶液呈碱性,所以c(H+)<c(OH-),根据电荷守恒得c(NH4+)>c(Cl-),错误;B.0.2 mol?L-1的CH3COONa溶液与0.1 mol?L-1的HCl等体积混合,溶液中的溶质是等物质的量浓度的CH3COONa、NaCl和CH3COOH,CH3COOH的电离程度大于醋酸根离子水解程度,溶液呈酸性,c(H+)>c(OH-),醋酸电离程度大于醋酸根离子水解,所以c(Cl-)<c(CH3COO-),错误;C.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(CN-)+c(OH-)=c(Na+)+c(H+),错误;D.铝离子抑制铵根离子水解、醋酸根离子促进铵根离子水解、一水合氨电离程度较小,所以相同浓度的这几种溶液中,盐完全电离、一水合氨部分电离,抑制铵根离子水解的溶液中铵根离子浓度大于促进水解的溶液,则这几种溶液中铵根离子浓度大小顺序是NH4Al(SO4)2>NH4Cl>CH3COONH4>NH3?H2O,正确。
考点:考查离子浓度大小比较。

(18分)已知25 ℃时部分弱电解质的电离平衡常数数据如下表:
弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
电离平衡常数 | 1.3×10-1 | 1.7×10-5 | 6.2×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
回答下列问题:
(1)写出碳酸的第一级电离平衡常数表达式:K1=_______________________。
(2)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为___ _____(填字母)。
(3)常温下,0.1 mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是 (填序号)
A.[H+] B.[H+]/[CH3COOH] C.[H+]·[OH-] D.[OH-]/[H+]
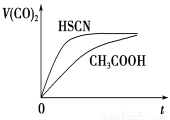
(4)25 ℃时,将20 mL 0.1 mol·L-1 CH3COOH溶液和20mL0.1 mol·L -1HSCN溶液分别与20 mL 0.1 mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是 反应结束后所得两溶液中,c(CH3COO-)________c(SCN-)(填“>”、“<”或“=”)
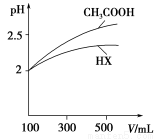
(5)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
(6)25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=________mol·L-1(填精确值),
c(CH3COO-)/c(CH3COOH)=________。
(7)写出少量CO2通入次氯酸钠溶液中的离子方程式:_____________________________。
