��Ŀ����
��18�֣���֪25 ��ʱ����������ʵĵ���ƽ�ⳣ���������±���
���ữѧʽ | HSCN | CH3COOH | HCN | H2CO3 |
����ƽ�ⳣ�� | 1.3��10��1 | 1.7��10��5 | 6.2��10��10 | K1��4.3��10��7 K2��5.6��10��11 |
�ش��������⣺
��1��д��̼��ĵ�һ������ƽ�ⳣ������ʽ��K1��_______________________��
��2�������ʵ���Ũ�ȵ�a.CH3COONa��b.NaCN��c.Na2CO3��d.NaHCO3��Һ��pH�ɴ�С��˳��Ϊ___ _____(����ĸ)��
��3�������£�0.1 mol��L��1��CH3COOH��Һ��ˮϡ�����У����б���ʽ�����ݱ����� (�����)
A��[H��] B��[H��]/[CH3COOH] C��[H��]��[OH��] D��[OH��]/[H��]
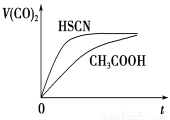
��4��25 ��ʱ����20 mL 0.1 mol��L��1 CH3COOH��Һ��20mL0.1 mol��L ��1HSCN��Һ�ֱ���20 mL 0.1 mol��L��1NaHCO3��Һ��ϣ�ʵ���ò������������(V)��ʱ��(t)�ı仯��ͼ��ʾ����Ӧ��ʼ��������Һ����CO2��������ʴ������Բ����ԭ���� ��Ӧ��������������Һ�У�c(CH3COO��)________c(SCN��)(�����������������)
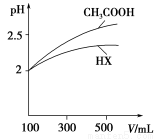
��5�������Ϊ100 mL pH��2��CH3COOH��һԪ��HX����ˮϡ������pH����Һ����Ĺ�ϵ��ͼ��ʾ����HX�ĵ���ƽ�ⳣ��________(����ڡ�����С�ڡ����ڡ�)CH3COOH�ĵ���ƽ�ⳣ����
��6��25 ��ʱ����CH3COOH��CH3COONa�Ļ����Һ�У������pH��6������Һ��c(CH3COO��)��c(Na��)��________mol��L��1(�ȷֵ)��
c(CH3COO��)/c(CH3COOH)��________��
��7��д������CO2ͨ�����������Һ�е����ӷ���ʽ��_____________________________��
��1�� ��2��cbda ��3��BD ��4��ͬŨ�ȵ�HSCN��CH3COOH����ǿ������Һ�е�c(H��)�ϴ���NaHCO3��Һ��Ӧ�� < ��5��С��
��2��cbda ��3��BD ��4��ͬŨ�ȵ�HSCN��CH3COOH����ǿ������Һ�е�c(H��)�ϴ���NaHCO3��Һ��Ӧ�� < ��5��С��
��6��9.9��10��7 17 ��7��CO2��H2O��ClO��===HCO3-��HClO
��������
�����������1��̼��ĵ���H2CO3 = H+ + HCO3- ��HCO3- = H+ + CO32- ����һ������ƽ�ⳣ������ʽ��K1��  ��2������ƽ�ⳣ��ԽС����Խ������˸��ݵ���ƽ�ⳣ����֪������ǿ��˳����HSCN��CH3COOH��H2CO3��HCN��HCO3������Խ������Ӧ������Խ����ˮ�⣬��Һ��pHԽ��������ʵ���Ũ�ȵ�a.CH3COONa��b.NaCN��c.Na2CO3��d.NaHCO3��Һ��pH�ɴ�С��˳��Ϊc��b��d��a����3�� A.0.1mol?L-1��CH3COOH��Һ��ˮϡ�ͣ���Һ���Լ�����c��H+����С��B������ĵ���̶�������Һ��n��H+������n��CH3COOH����С��Ũ��֮�ȵ������ʵ���֮�ȣ�[H��]/[CH3COOH]����C��һ���¶���c��H+��?c��OH-��Ϊ��ֵ��D.0.1mol?L-1��CH3COOH��Һ��ˮϡ�ͣ���Һ���Լ�����c��H+����С��c��OH-������[OH��]/[H��]����4�� ���ݵ��볣����֪��ͬŨ�ȵ�HSCN��CH3COOH����ǿ��������NaHCO3��Һ��Ӧ�죻��Ӧ������õ����Ǵ����ƺ�NaSCN��Һ������������HSCN��CH3COOH����ǿ�����Դ����Ƶ�ˮ��̶�ǿ��NaSCN��ˮ��̶ȣ������Һ��c��CH3COO������c��SCN��������5������CH3COOH��һԪ��HX��ˮϡ������pH����Һ����Ĺ�ϵͼ���Կ���HX����ϡ��������Һ��PH�仯�ȴ���Ĵ���������HXǿ�ڴ��ᣬ����̶ȣ�HX��CH3COOH������ƽ�ⳣ����6�� 4��CH3COOH��CH3COONa�Ļ����Һ�У����ڵ���غ㣺c��Na+��+c��H+��=c��OH����+c��CH3COO����������c��CH3COO������c��Na+��=c��H+����c��OH����=10��6mol/L��10��8mol/L=9.9��10��7mol/L����7�� ��ĵ��볣��Խ������Խǿ����������ǿ��˳����H2CO3��HClO��HCO3-��������ǿ��˳���֪������CO2ͨ�����������Һ�е����ӷ���ʽ��CO2��H2O��ClO��===HCO3-��HClO��
��2������ƽ�ⳣ��ԽС����Խ������˸��ݵ���ƽ�ⳣ����֪������ǿ��˳����HSCN��CH3COOH��H2CO3��HCN��HCO3������Խ������Ӧ������Խ����ˮ�⣬��Һ��pHԽ��������ʵ���Ũ�ȵ�a.CH3COONa��b.NaCN��c.Na2CO3��d.NaHCO3��Һ��pH�ɴ�С��˳��Ϊc��b��d��a����3�� A.0.1mol?L-1��CH3COOH��Һ��ˮϡ�ͣ���Һ���Լ�����c��H+����С��B������ĵ���̶�������Һ��n��H+������n��CH3COOH����С��Ũ��֮�ȵ������ʵ���֮�ȣ�[H��]/[CH3COOH]����C��һ���¶���c��H+��?c��OH-��Ϊ��ֵ��D.0.1mol?L-1��CH3COOH��Һ��ˮϡ�ͣ���Һ���Լ�����c��H+����С��c��OH-������[OH��]/[H��]����4�� ���ݵ��볣����֪��ͬŨ�ȵ�HSCN��CH3COOH����ǿ��������NaHCO3��Һ��Ӧ�죻��Ӧ������õ����Ǵ����ƺ�NaSCN��Һ������������HSCN��CH3COOH����ǿ�����Դ����Ƶ�ˮ��̶�ǿ��NaSCN��ˮ��̶ȣ������Һ��c��CH3COO������c��SCN��������5������CH3COOH��һԪ��HX��ˮϡ������pH����Һ����Ĺ�ϵͼ���Կ���HX����ϡ��������Һ��PH�仯�ȴ���Ĵ���������HXǿ�ڴ��ᣬ����̶ȣ�HX��CH3COOH������ƽ�ⳣ����6�� 4��CH3COOH��CH3COONa�Ļ����Һ�У����ڵ���غ㣺c��Na+��+c��H+��=c��OH����+c��CH3COO����������c��CH3COO������c��Na+��=c��H+����c��OH����=10��6mol/L��10��8mol/L=9.9��10��7mol/L����7�� ��ĵ��볣��Խ������Խǿ����������ǿ��˳����H2CO3��HClO��HCO3-��������ǿ��˳���֪������CO2ͨ�����������Һ�е����ӷ���ʽ��CO2��H2O��ClO��===HCO3-��HClO��
���㣺����������ʵĵ��롢����ˮ�⡢��Һ������Ũ�ȴ�С�Ƚϡ�

 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д� ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д������£�������4����Һ������˵����ȷ����
�� | �� | �� | �� |
0.1 mol��L��1 CH3COOH��Һ | pH��3 CH3COOH��Һ | 0.1 mol ��L��1 NaOH��Һ | pH��11 NaOH��Һ |
A����ˮ�������c(H��)���ۣ���
B����ϡ�͵�ԭ����100����pH�����ͬ
C������ۻ�ϣ�����ҺpH��7����������Һ��������ۣ���
D������ܻ�ϣ�����ҺpH��7����������Һ��������ܣ���