题目内容
15. 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题(1)该反应是放热反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率减小(填“增大”“减小”“不变”),原因是该反应正反应为放热反应,升高温度使平衡向逆反应方向移动.
(3)反应体系中加入催化剂对反应热是否有影响?否,催化剂只改变反应活化能,不改变反应物和生物成的能量,
(4)在反应体系中加入催化剂,反应速率增大,E1的变化是:E1减小,(填“增大”“减小”“不变”)
分析 (1)根据反应物总能量和生成物总能量的关系判断反应热;
(2)升高温度使平衡向逆反应方向移动;
(3)催化剂对平衡无影响;
(4)加入催化剂能降低物质的活化能.
解答 解:(1)由图象可以看出反应物总能量大于生成物的总能量,则该反应的正反应为放热反应,故答案为:放热;
(2)当反应达到平衡时,该反应正反应为放热反应,升高温度使平衡向逆反应方向移动,A的转化率减小,故答案为:减小;该反应正反应为放热反应,升高温度使平衡向逆反应方向移动;
(3)催化剂能加快反应速率但不改变平衡的移动,所以反应热不变,故答案为:否,催化剂只改变反应活化能,不改变反应物和生物成的能量;
(4)加入催化剂能降低反应物质的活化能,则E1和E2都减小,故答案为:减小.
点评 本题考查反应热的判断,影响化学反应速率的因素,注意知识的迁移应用是关键,难度适中.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
5.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 500 mL1 mol/L MgCl2溶液中含有Cl-数目为0.5NA | |
| B. | 标准状况下,33.6L SO3与48gO2所占的体积相等 | |
| C. | 17 gNH3含有的电子个数为l0NA | |
| D. | 1 mol O2与2 mol SO2一定条件下混合反应,可生成2 mol SO3 |
6.元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中只有X是短周期的金属元素,下列判断正确的是( )
| R | ||
| X | T | Z |
| Q |
| A. | X的最高价氧化物能溶于强碱 | B. | 非金属性:T>R | ||
| C. | 单质导电性:Z>T>X | D. | R与Q的原子核外电子数相差16 |
10.常温下,向20.00mL 0.100 0mol•L-1 的CH3COONa溶液中逐滴加入0.100 0mol•L-1盐酸,溶液的pH与所加盐酸体积的关系如图所示(不考虑挥发),下列说法正确的是( )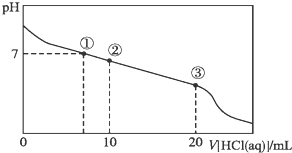

| A. | 点①所示溶液中,溶质为未反应完的CH3COONa、生成的CH3COOH和NaCl,微粒之间的关系为:c(CH3COOH)>c(Cl-)>c(OH-)=c(H+) | |
| B. | 点②所示溶液中,醋酸钠有一半与盐酸反应,微粒之间的关系为:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH) | |
| C. | 点③所示溶液中,醋酸钠与盐酸恰好完全反应,微粒之间的关系为:c(Na+)>c(CH3COOH)>c(H+)>c(CH3COO-) | |
| D. | 整个过程中有可能出现:c(H+)+c(Na+)=c(CH3COOH)+c(CH3COO-) |
5.用四种溶液进行实验,下表中“操作及现象“与”溶液“对应关系错误的是( )
| 选项 | 操作及现象 | 溶液 |
| A | 通入二氧化碳,溶液变浑浊 | 饱和碳酸钠溶液 |
| B | 通入二氧化碳,溶液变浑浊,继续通二氧化碳至过量,浑浊消失 | 硅酸钠溶液 |
| C | 通入二氧化碳,溶液变浑浊,继续通二氧化碳至过量,浑浊消失,再加入足量氢氧化钠溶液,又变浑浊 | 澄清石灰水 |
| D | 通入二氧化碳,溶液变浑浊,再加入品红溶液,红色褪色 | 次氯酸钙溶液 |
| A. | A | B. | B | C. | C | D. | D |
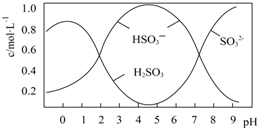 葡萄酒常用Na2S2O5做抗氧化剂.
葡萄酒常用Na2S2O5做抗氧化剂.