题目内容
16.NA为阿伏加德罗常数,下列叙述错误的是( )| A. | 18g H2O中含有的质子数为10NA | |
| B. | 标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA | |
| C. | 46g NO2和N2O4混合气体中含有原子总数为3NA | |
| D. | 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
分析 A、求出水的物质的量,然后根据水为10质子微粒来分析;
B、标况下氯仿为液态;
C、NO2和N2O4的最简式均为CH2;
D、根据反应后钠元素的价态为+1价来分析.
解答 解:A、18g水的物质的量为1mol,而水为10质子微粒,故1mol水中含10mol质子即10NA个,故A正确;
B、标况下氯仿为液态,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、NO2和N2O4的最简式均为NO2,故46g混合物中含有的NO2的物质的量为n=$\frac{46g}{46g/mol}$=1mol,则含3mol原子即3NA个,故C正确;
D、由于反应后钠元素的价态为+1价,故1mol钠失去1mol电子即NA个,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
7.下列叙述错误的是( )
| A. | 置换反应一定是氧化还原反应 | |
| B. | 二氧化碳是非电解质 | |
| C. | 等质量的二氧化硫和氨气,前者体积大 | |
| D. | 坩埚、试管、蒸发皿都可以用酒精灯直接加热 |
11.NA表示阿伏伽德罗常数,下列说法不正确的是( )
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 常温常压下,92g的NO2和N2O4混合气体中含有的原子总数为6NA | |
| C. | 在Fe与CuSO4溶液的反应中,有1molFe参加反应,转移电子数为3NA | |
| D. | 1mol K2SO4中阴离子所带电荷数为2NA |
1.工业上用白云石制备高纯氧化镁的工艺流程如图:

已知Ⅰ.白云石主要成分可表示为:CaO 32.50%;MgO 20.58%;Fe2O32.18%;SiO2 0.96%;其他 43.78%.
(1)若在实验室中煅烧白云石,需要的仪器除酒精灯、三脚架以外,还需要BC(填序号).
A.蒸发皿 B.坩埚 C.泥三角 D.石棉网
(2)加入H2SO4控制pH时,终点pH对产品的影响如图所示.则由图示可得到的结论及原因是:

①pH过高会导致镁浸出率降低,
②pH过低会引起产品纯度下降,其原因可能是AC(填序号)
A.Fe2O3溶于H2SO4最终使产品混有杂质
B.SiO2溶于H2SO4最终使产品混有杂质
C.酸性过强,形成可溶的Ca(HSO4)2,最终使产品混有含钙的杂质
(3)已知MgSO4、CaSO4的溶解度如表:
根据上表数据,简要说明析出CaSO4•2H2O的操作步骤是升温结晶、趁热过滤.
(4)该生产流程中还可得到的一种用途很大的副产品是硫酸铵.

已知Ⅰ.白云石主要成分可表示为:CaO 32.50%;MgO 20.58%;Fe2O32.18%;SiO2 0.96%;其他 43.78%.
(1)若在实验室中煅烧白云石,需要的仪器除酒精灯、三脚架以外,还需要BC(填序号).
A.蒸发皿 B.坩埚 C.泥三角 D.石棉网
(2)加入H2SO4控制pH时,终点pH对产品的影响如图所示.则由图示可得到的结论及原因是:

①pH过高会导致镁浸出率降低,
②pH过低会引起产品纯度下降,其原因可能是AC(填序号)
A.Fe2O3溶于H2SO4最终使产品混有杂质
B.SiO2溶于H2SO4最终使产品混有杂质
C.酸性过强,形成可溶的Ca(HSO4)2,最终使产品混有含钙的杂质
(3)已知MgSO4、CaSO4的溶解度如表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(4)该生产流程中还可得到的一种用途很大的副产品是硫酸铵.
8.下列叙述正确的是( )
| A. | 硫酸钡难溶于水,在水溶液中不能导电,所以硫酸钡不是电解质 | |
| B. | 强电解质在水溶液中的导电性一定比弱电解质强 | |
| C. | 三氧化硫溶于水能导电,所以三氧化硫是电解质 | |
| D. | 硫酸、氢氧化钡、纯碱、苛性钠都是强电解质 |
5.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1 CH3COONa溶液与0.1 mol•L-1 HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | 0.1 mol•L-1 NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH${\;}_{4}^{+}$)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液与0.1 mol•L-1 NaHCO3溶液等体积混合:3c(Na+)=2c(CO${\;}_{3}^{2-}$)+2c(HCO${\;}_{3}^{-}$)+2c(H2CO3) | |
| D. | 0.1 mol•L-1 Na2C2O4溶液与0.1 mol•L-1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O${\;}_{4}^{2-}$)+c(HC2O${\;}_{4}^{-}$)+c(OH-)=c(H+)+c(Cl-) |

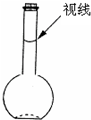 实验室配制500mL 0.5mol•L-1的NaCl溶液,有如下操作步骤:
实验室配制500mL 0.5mol•L-1的NaCl溶液,有如下操作步骤: