题目内容
5.下列反应的离子方程式中,错误的是( )| A. | 铁跟稀硫酸反应 Fe+2H+═Fe2++H2↑ | |
| B. | 碳酸氢钙溶液跟盐酸反应 Ca(HCO3)2+2H+═Ca2++2H2O+2CO2↑ | |
| C. | 醋酸跟氢氧化钾溶液反应 CH3COOH+OH-═CH3COO-+H2O | |
| D. | 碳酸镁跟硫酸反应 MgCO3+2H+═Mg2++H2O+CO2↑ |
分析 A.稀硫酸具有弱氧化性,能将铁氧化为亚铁离子;
B.碳酸钙是可溶性盐,应该写离子;
C.醋酸和KOH反应生成醋酸钾和水;
D.碳酸镁和稀硫酸反应生成硫酸镁、二氧化碳和水.
解答 解:A.稀硫酸具有弱氧化性,能将铁氧化为亚铁离子,离子方程式为Fe+2H+═Fe2++H2↑,故A正确;
B.碳酸钙是可溶性盐,应该写离子,离子方程式为HCO3-+H+═H2O+CO2↑,故B错误;
C.醋酸和KOH反应生成醋酸钾和水,离子方程式为CH3COOH+OH-═CH3COO-+H2O,故C正确;
D.碳酸镁和稀硫酸反应生成硫酸镁、二氧化碳和水,离子方程式为MgCO3+2H+═Mg2++H2O+CO2↑,故D正确;
故选B.
点评 本题考查离子方程式正误判断,为高频考点,侧重考查学生分析判断及应用能力,明确离子方程式书写特点及物质性质是解本题关键,单质、氧化物、气体、沉淀、弱电解质都写化学式,易错选项是C.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.下列物质中属于电解质的是( )
①氢氧化钠 ②氯化钠溶液 ③铜 ④蔗糖 ⑤二氧化碳 ⑥硫酸钡.
①氢氧化钠 ②氯化钠溶液 ③铜 ④蔗糖 ⑤二氧化碳 ⑥硫酸钡.
| A. | ①②⑥ | B. | ①②⑤ | C. | ③④ | D. | ①⑥ |
16.下列反应是氧化还原反应,且水既不做氧化剂,又不做还原剂的是( )
| A. | NaH+H2O═NaOH+H2↑ | B. | F2+2H2O═2O2↑+4HF | ||
| C. | 2Na2O2+2H2O═4NaOH+O2↑ | D. | Mg2N2+6H2O═3Mg(OH)2+2NH3↑ |
13.下列除杂试剂选择不合理的是( )
| A. | NaOH(Na2CO3):适量Ba(OH)2溶液 | |
| B. | NaCl(Na2CO3):适量CaCl2溶液 | |
| C. | KCl(FeCl3):适量Ba(OH)2溶液 | |
| D. | KNO3(Ba(NO3)2):先加适量K2CO3溶液,再加适量HN03 |
20.下面关于氢化物的叙述正确的是( )
| A. | 一个D2O分子所含的中子数为8 | B. | NH3的结构式为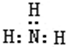 | ||
| C. | HCl的电子式为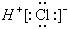 | D. | 热稳定性:H2S<HF |
10.下列叙述中,正确的是( )
| A. | 硫酸的摩尔质量是98g | B. | 1mol N2的质量为28g/mol | ||
| C. | 阿伏伽德罗常数用符号为NA表示 | D. | 1mol氧的质量等于16g |
17.下列化学用语正确的是( )
| A. | NaHCO3 的电离:NaHCO3?Na++H++CO${\;}_{3}^{2-}$ | |
| B. | HS-的电离:HS-+H2O?H3O++S2- | |
| C. | H3PO4的电离:H3PO4?3H++PO${\;}_{4}^{3-}$ | |
| D. | 熔融状态下NaHSO4的电离:NaHSO4═Na++SO${\;}_{4}^{2-}$ |
15.铜、汞、铅等重金属盐能使人中毒,如误入口应采取急救措施的是( )
| A. | 喝大量蒸馏水 | B. | 喝大量盐水 | C. | 喝大量鸡蛋清 | D. | 喝大量葡萄糖水 |
