题目内容
2.橙花醇具有玫瑰及苹果香气,可作为香料.其结构简式如图:
下列关于橙花醇的叙述,错误的是( )
| A. | 既能发生取代反应,也能发生加成反应 | |
| B. | 在浓硫酸催化下加热脱水,可以生成不止一种四烯烃 | |
| C. | 1mol橙花醇在氧气中充分燃烧,需消耗448 L氧气(标准状况) | |
| D. | 1mol橙花醇在室温下与溴的四氯化碳溶液反应,最多消耗3mol溴 |
分析 该有机物含有碳碳双键,可发生加成、加聚、氧化反应,含有羟基,可发生氧化、消去和取代反应,以此解答该题.
解答 解:A.该有机物含有羟基,可发生取代反应,含有碳碳双键,可发生加成反应,故A正确;
B.在浓硫酸催化下加热脱水,发生消去反应,能生成2种四烯烃,故B错误;
C.分子式为C15H26O,1 mol橙花醇在氧气中充分燃烧,需消耗氧气(15+$\frac{26}{4}$-$\frac{1}{2}$)mol=21mol,体积为21mol×22.4mol/L=470.4 L,故C错误;
D.有机物中含有3个碳碳双键,则1mo1橙花醇在室温下与溴四氯化碳溶液反应,最多消耗3mol溴,故D正确.
故选BC.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于有机物知识的综合应用,题目难度中等,易错点为D,注意把握有机物的结构特点.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
12.下列物质中只含有离子键的是( )
| A. | CS2 | B. | Na2O2 | C. | CaO | D. | CH3COOH |
13.下列物质中,不属于通常所说的三大合成材料的是( )
| A. | 塑料 | B. | 蛋白质 | C. | 合成纤维 | D. | 合成橡胶 |
10.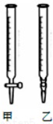 某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是(填编号)①.
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入乙中.(从图中选填“甲”或“乙”)
(3)下列操作会引起实验结果偏大的是:B(填编号)
A.在锥形瓶装液前,留有少量蒸馏水
B.滴定前,滴定管尖嘴有气泡,滴定后无气泡
C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D.用酸式滴定管量取液体时,释放液体前滴定管前端有气泡,之后消失
(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视锥形瓶内颜色.判断到达滴定终点的现象是:锥形瓶中溶液由无色变成浅红色,且半分钟内不变色.
(5)以下是实验数据记录表
通过计算可得,该盐酸浓度为:0.1631 mol•L-1(计算结果保留4位小数)
 某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是(填编号)①.
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入乙中.(从图中选填“甲”或“乙”)
(3)下列操作会引起实验结果偏大的是:B(填编号)
A.在锥形瓶装液前,留有少量蒸馏水
B.滴定前,滴定管尖嘴有气泡,滴定后无气泡
C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D.用酸式滴定管量取液体时,释放液体前滴定管前端有气泡,之后消失
(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视锥形瓶内颜色.判断到达滴定终点的现象是:锥形瓶中溶液由无色变成浅红色,且半分钟内不变色.
(5)以下是实验数据记录表
| 滴定次数 | 盐酸体积mL | NaOH溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 21.30 |
| 2 | 20.00 | 0.00 | 16.30 |
| 3 | 20.00 | 0.00 | 16.32 |
17.下列各组离子在溶液中能大量共存,加入 Fe2(SO4)3后仍能大量共存的是( )
| A. | Na+、I-、CO32-、ClO- | B. | Ba2+、Na+、SCN-、Cl- | ||
| C. | Fe2+、H+、K+、NO3- | D. | Cu2+、Mg2+、Cl-、NO3- |
7.下列叙述中错误的是( )
| A. | 煤是工业上获得苯、甲苯、二甲苯等芳香烃的重要来源物质 | |
| B. | 海水提溴、海带提碘的过程均不涉及化学变化 | |
| C. | 铝热反应放出大量的热,金属铝做还原剂 | |
| D. | 通过催化重整,可从石油中获取环状烃 |
14.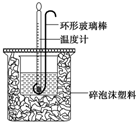 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据
(1)碎泡沫塑料的作用是保温隔热,减少热量损失环形玻璃搅拌棒可不可以用铜丝搅拌棒代替,为什么不可以;铜的导热性好,易损失热量产生误差
(2)该实验测得的中和热数值为56.8 kJ•mol-1,(盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算).
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热的数值偏小(“偏大”、“偏小”或“不变”)
 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃[来源:Z,xx,k.Com] | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.3 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 20.5 | 20.6 | 24.9 |
(2)该实验测得的中和热数值为56.8 kJ•mol-1,(盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算).
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热的数值偏小(“偏大”、“偏小”或“不变”)
2.某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行滴定操作:
选用仪器如下:①量筒;②锥形瓶;③滴定管;④玻璃棒.上列仪器中在使用前需检查是否漏水的是③.(填序号)除以上仪器外还缺的玻璃仪器有250mL容量瓶中、胶头滴管.
操作步骤:
A.在250mL容量瓶中配制250mL烧碱溶液
B.用碱式滴定管量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品w g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为m mol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1 mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
附:酸碱指示剂变色范围
请完成下列问题:
(1)正确的操作步骤是(填写字母)C→A→B→D→E.
(2)滴定管读数应注意滴定管垂直,液面不再变化时才可读数,视线与溶液凹液面最低点相平,读数精确到0.01ml.
(3)操作中锥形瓶下垫一张白纸的作用是便于准确判断终点时颜色的变化情况.
(4)操作D中液面应调整到调节到零刻度或零稍下的某一刻度,充满标准H2SO4溶液;
(5)滴定到终点时锥形瓶内溶液的pH约为4;终点时的颜色变化是溶液由黄色变为橙色,且半分钟内不恢复为原来的颜色.
(6)若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响偏高(填“偏高”、“偏低”或“无影响”,其他操作均正确).
选用仪器如下:①量筒;②锥形瓶;③滴定管;④玻璃棒.上列仪器中在使用前需检查是否漏水的是③.(填序号)除以上仪器外还缺的玻璃仪器有250mL容量瓶中、胶头滴管.
操作步骤:
A.在250mL容量瓶中配制250mL烧碱溶液
B.用碱式滴定管量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品w g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为m mol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1 mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
附:酸碱指示剂变色范围
| 指示剂 | 变色范围 | 酸色 | 碱色 |
| 石蕊 | 5.0-8.0 | 红色 | 蓝色 |
| 酚酞 | 8.0-10.0 | 无色 | 红色 |
| 甲基橙 | 3.1-4.4 | 红色 | 黄色 |
(1)正确的操作步骤是(填写字母)C→A→B→D→E.
(2)滴定管读数应注意滴定管垂直,液面不再变化时才可读数,视线与溶液凹液面最低点相平,读数精确到0.01ml.
(3)操作中锥形瓶下垫一张白纸的作用是便于准确判断终点时颜色的变化情况.
(4)操作D中液面应调整到调节到零刻度或零稍下的某一刻度,充满标准H2SO4溶液;
(5)滴定到终点时锥形瓶内溶液的pH约为4;终点时的颜色变化是溶液由黄色变为橙色,且半分钟内不恢复为原来的颜色.
(6)若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响偏高(填“偏高”、“偏低”或“无影响”,其他操作均正确).
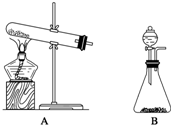 氨气是化学实验室常需制取的气体.实验室制取氨气通常有两种方法:
氨气是化学实验室常需制取的气体.实验室制取氨气通常有两种方法: