题目内容
14.下列说法中,正确的是( )| A. | 甲醇、乙二醇、丙三醇都易溶于水且都有剧毒 | |
| B. | 按甲醇、乙二醇、丙三醇的顺序,其沸点逐渐升高 | |
| C. | 相同质量的甲醇、乙二醇、丙三醇与足量钠反应,甲醇放出氢气最多 | |
| D. | 甲醇、乙二醇、丙三醇都能发生取代、消去、氧化反应 |
分析 A.均含-OH,易形成氢键,只有甲醇有毒;
B.含-OH越多,沸点越大;
C.相等质量各醇与氢气反应,醇中羟基质量分数越大,生成氢气越多;
D.均含-OH可发生氧化、取代反应,只有甲醇不能发生消去反应.
解答 解:A.均含-OH,易形成氢键,则甲醇、乙二醇、丙三醇都易溶于水,只有甲醇有毒,故A错误;
B.含-OH越多,沸点越大,则按甲醇、乙二醇、丙三醇的顺序,其沸点逐渐升高,故B正确;
C.甲醇为CH3OH,乙二醇为HOCH2CH2OH,丙三醇为HOCH2CH(OH)CH2OH,羟基质量分数为:丙三醇>乙二醇>甲醇,故丙三醇生成氢气最多,故C错误;
D.均含-OH可发生氧化、取代反应,只有甲醇(没有邻位C)不能发生消去反应,而乙二醇、丙三醇都能发生消去反应,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重醇的性质及分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
4.下列有机物命名正确的是( )
| A. |  2-乙基丙烷 2-乙基丙烷 | B. | 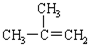 2-甲基-2-丙烯 2-甲基-2-丙烯 | ||
| C. | 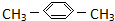 间二甲苯 间二甲苯 | D. | CH3CH2CH2CH2OH 1-丁醇 |
5. 质子交换膜燃料电池(proton exchange membrane fuel cell,英文简称PEMFC)是燃料电池的一种.如图是质子交换膜氢氧燃料电池,下列有关该电池的原理的描述正确的是( )
质子交换膜燃料电池(proton exchange membrane fuel cell,英文简称PEMFC)是燃料电池的一种.如图是质子交换膜氢氧燃料电池,下列有关该电池的原理的描述正确的是( )
 质子交换膜燃料电池(proton exchange membrane fuel cell,英文简称PEMFC)是燃料电池的一种.如图是质子交换膜氢氧燃料电池,下列有关该电池的原理的描述正确的是( )
质子交换膜燃料电池(proton exchange membrane fuel cell,英文简称PEMFC)是燃料电池的一种.如图是质子交换膜氢氧燃料电池,下列有关该电池的原理的描述正确的是( )| A. | 溶液中H+透过质子交换膜从右向左迁移 | |
| B. | 正极反应式为:O2+2H2O+4e-=4OH- | |
| C. | 电子从a极流出经电解质溶液流到b极 | |
| D. | 该电池在使用过程中,H+的物质的量保持不变 |
2.下列说法正确的是( )
| A. | 人们常借助元素分析仪来确定有机化合物的组成 | |
| B. | 有机化合物的核磁共振氢谱可以帮助我们确定物质中氢原子的种类 | |
| C. | 根据对红外光谱的分析,可以初步判定该有机物中碳原子的种类 | |
| D. | 用质谱法对有机物进行分析,可以初步判断该有机物中具有哪些基团 |
9.下列物质中,只含有非极性共价键的是( )
| A. | Na2O2 | B. | NaOH | C. | O3 | D. | H2S |
19.电负性的大小也可以作为判断元素金属性和非金属性强弱的尺度.下列关于电负性的变化规律正确的是( )
| A. | 周期表从左到右,元素的电负性逐渐变大 | |
| B. | 周期表从上到下,元素的电负性逐渐变大 | |
| C. | 电负性越大,金属性越强 | |
| D. | 电负性越小,非金属性越强 |
6.下列有关浓硫酸和亚硫酸钠混和放出的气体的说法中不正确的是( )
| A. | 它与氧气接触即转变为SO3 | |
| B. | 亚硫酸钙能溶解于它的水溶液中 | |
| C. | 它的密度比空气小,且不易液化 | |
| D. | 它的水溶液是酸性,且能被强氧化剂氧化 |
3.下列关于苯酚的叙述中,错误的是( )
| A. | 碳酸氢钠溶液中滴入苯酚的水溶液后不会放出二氧化碳 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 其在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶 | |
| D. | 其水溶液显强酸性,俗称石炭酸 |
4.某元素的结构示意图如图所示,该元素在周期表中位于第几周期,( )
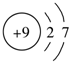

| A. | 一 | B. | 二 | C. | 三 | D. | 四 |