题目内容
9.下列物质中,只含有非极性共价键的是( )| A. | Na2O2 | B. | NaOH | C. | O3 | D. | H2S |
分析 从极性共价键和非极性共价键的概念判断,同种元素的原子间形成的共价键,共用电子对在成键两原子的中间,不向任何一方偏转,这种共价键叫非极性键;不同种元素的原子间形成的键,都是极性键.
解答 解:A.Na2O2为离子化合物,含有离子键和非极性共价键,故A错误;
B.NaOH为离子化合物,含有离子键和极性共价键,故B错误;
C.只含有O-O键,形成的共价键的原子相同,为非极性共价键,故C正确;
D.H2S中形成的共价键的原子不相同,为极性共价键,故D错误.
故选C.
点评 本题考查共价键知识,为高频考点,侧重于双基的考查,注意非极性键可存在于单质分子中(如H2中H-H键、O2中O=O键、N2中N≡N键),分子结构比较对称的两种非金属元素组成的化合物也具有非极性共价键(如:C2H2,C2H4,C6H6等).

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
14.下列说法中,正确的是( )
| A. | 甲醇、乙二醇、丙三醇都易溶于水且都有剧毒 | |
| B. | 按甲醇、乙二醇、丙三醇的顺序,其沸点逐渐升高 | |
| C. | 相同质量的甲醇、乙二醇、丙三醇与足量钠反应,甲醇放出氢气最多 | |
| D. | 甲醇、乙二醇、丙三醇都能发生取代、消去、氧化反应 |
1.将等物质的量的A、B混合于2L的恒容密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(g),经5min后,测得D的量为1mol,C的平均反应速率是0.1mol/(L•min).则x的值为( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
18.下列说法正确的一组是( )
①不溶于水的盐(CaCO3、BaSO4等)都是弱电解质
②二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质
③氯化钠水溶液在电流的作用下电离出Na+和Cl-,所以氯化钠是强电解质
④强酸溶液中氢离子浓度一定大于弱酸溶液中氢离子浓度
⑤熔融的电解质都能导电
⑥强电解质可能是离子化合物,也可能是共价化合物.
①不溶于水的盐(CaCO3、BaSO4等)都是弱电解质
②二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质
③氯化钠水溶液在电流的作用下电离出Na+和Cl-,所以氯化钠是强电解质
④强酸溶液中氢离子浓度一定大于弱酸溶液中氢离子浓度
⑤熔融的电解质都能导电
⑥强电解质可能是离子化合物,也可能是共价化合物.
| A. | ①③⑤⑥ | B. | ②④⑤⑥ | C. | 只有⑤ | D. | 只有⑥ |
19.短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法正确的是( )


| A. | X、Y、Z三种元素中,X的非金属性最强 | |
| B. | Y的氢化物的稳定性比Z的氢化物弱 | |
| C. | Y的最高正化合价为+7 | |
| D. | X的单质的熔点比Z的低 |
 (X)为卤素原子.
(X)为卤素原子.
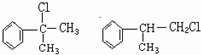 ;
; ;
; +NaOH$\stackrel{△}{→}$
+NaOH$\stackrel{△}{→}$ +NaCl;
+NaCl; 或
或 .
.
 CH3COOC2H5+H2O
CH3COOC2H5+H2O 如图所示装置,c、d两极是石墨电极,回答下列问题:
如图所示装置,c、d两极是石墨电极,回答下列问题: