题目内容
A、B是短周期元素,最外层电子排布式分别为msx,nsxnpx+1.A与B形成的离子化合物加蒸馏水溶解后可使酚酞试液变红,同时有气体逸出,该气体可使湿润的红色石蕊试纸变蓝,则该化合物的相对分子质量是( )
| A、38 | B、55 |
| C、100 | D、135 |
考点:原子结构与元素的性质
专题:原子组成与结构专题
分析:A、B是短周期元素,最外层电子排布式分别为msx,nsxnpx+1,由B的最外层电子排布式nsxnpx+1可知ns已经排满,则x=2,则A、B最外层电子排布式分别为ms2,ns2np3,
则A为第IIA族元素,B为第VA族元素,A与B形成的离子化合物加蒸馏水溶解后可使酚酞试液变红,同时有气体逸出,该气体可使湿润的红色石蕊试纸变蓝,则该气体为氨气,说明B为N元素,A、B是短周期元素,则A为Mg元素.
则A为第IIA族元素,B为第VA族元素,A与B形成的离子化合物加蒸馏水溶解后可使酚酞试液变红,同时有气体逸出,该气体可使湿润的红色石蕊试纸变蓝,则该气体为氨气,说明B为N元素,A、B是短周期元素,则A为Mg元素.
解答:
解:A、B是短周期元素,最外层电子排布式分别为msx,nsxnpx+1,由B的最外层电子排布式nsxnpx+1可知ns已经排满,则x=2,则A、B最外层电子排布式分别为ms2,ns2np3,则A为第IIA族元素,B为第VA族元素,A与B形成的离子化合物加蒸馏水溶解后可使酚酞试液变红,同时有气体逸出,该气体可使湿润的红色石蕊试纸变蓝,则该气体为氨气,说明B为N元素,A、B是短周期元素,则A为Mg元素,A与B形成的离子化合为Mg3N2,其化学式的式量为100,
故选C.
故选C.
点评:本题考查了元素的推断,侧重于考查最外层电子排布式、氨气的性质和检验、氢氧化镁的碱性等,明确核外电子排布规律是解题的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
有关Al与NaOH溶液的反应的说法中,正确的是( )
| A、铝是还原剂,其氧化产物是Al(OH)3 |
| B、NaOH是氧化剂,其还原产物是H2 |
| C、铝是还原剂,H2O和NaOH都是氧化剂 |
| D、H2O是氧化剂,Al被氧化 |
合成氨厂所需H2可由焦炭与水反应制得,其中有一步反应为CO(g)+H2O(g)═CO2(g)+H2(g)△H<0欲提高CO转化率,可采用的方法是( )
①降低温度;②增大压强;③使用催化剂;④增大CO浓度;⑤增大水蒸气浓度.
①降低温度;②增大压强;③使用催化剂;④增大CO浓度;⑤增大水蒸气浓度.
| A、①②③ | B、④⑤ | C、①⑤ | D、⑤ |
在0.1mol/L NaHCO3溶液中,下列关系式错误的是( )
| A、c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| B、c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-) |
| C、c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
| D、c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) |
下列物质的电子式书写正确的是( )
A、 |
B、 |
C、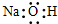 |
D、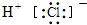 |
 夜幕降临,北京奥运会主会场“鸟巢”内灯火辉煌,鼓瑟齐鸣.璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应.鸟巢夜景照明由五个部分组成,其中主体照明以传统文化元素“中国红”为主色.请回答下列问题:
夜幕降临,北京奥运会主会场“鸟巢”内灯火辉煌,鼓瑟齐鸣.璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应.鸟巢夜景照明由五个部分组成,其中主体照明以传统文化元素“中国红”为主色.请回答下列问题: ,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题:
,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题: