题目内容
短周期元素X、Y、Z三种原子核外电子总数为32,都可形成常温下气体单质.X原子最外层电子数是其内层电子数的3倍;Y的气态氢化物与其最高价氧化物对应的水化物恰好反应的产物只有一种A,A的水溶液显酸性.下列说法正确的是( )
| A、原子半径:Z>X>Y |
| B、X元素形成的单质其摩尔质量一定是32g?moL-1 |
| C、物质A中既含离子键又含共价键 |
| D、YX2、ZX2都有对应的含氧酸 |
考点:原子结构与元素的性质
专题:
分析:短周期元素X、Y、Z三种原子核外电子总数为32,都可形成常温下气体单质,X原子的最外层电子数是其内层电子总数的3倍,X有2个电子层,最外层电子数为6,故X为O元素,Y的气态氢化物与其最高价氧化物对应的水化物恰好反应的产物只有一种A,A的水溶液显酸性,则A为硝酸铵,Y为N元素,Z的核外电子数=32-8-7=17,则Z为Cl元素,据此结合选项解答.
解答:
解:短周期元素X、Y、Z三种原子核外电子总数为32,都可形成常温下气体单质,X原子的最外层电子数是其内层电子总数的3倍,X有2个电子层,最外层电子数为6,故X为O元素,Y的气态氢化物与其最高价氧化物对应的水化物恰好反应的产物只有一种A,A的水溶液显酸性,则A为硝酸铵,Y为N元素,Z的核外电子数=32-8-7=17,则Z为Cl元素,
A.电子层数越多,半径越大,同周期自左而右原子半径减小,故原子半径Cl>N>O,即Z>Y>X,故A错误;
B.X为O元素,O元素形成的单质有氧气和臭氧其摩尔质量分别为32g?moL-1、48g?moL-1,故B错误;
C.A为硝酸铵,属于含氧酸盐,既含离子键又含共价键,故C正确;
D.YX2为NO2,ZX2为ClO2,二者没有有对应的含氧酸,故D错误;
故选:C.
A.电子层数越多,半径越大,同周期自左而右原子半径减小,故原子半径Cl>N>O,即Z>Y>X,故A错误;
B.X为O元素,O元素形成的单质有氧气和臭氧其摩尔质量分别为32g?moL-1、48g?moL-1,故B错误;
C.A为硝酸铵,属于含氧酸盐,既含离子键又含共价键,故C正确;
D.YX2为NO2,ZX2为ClO2,二者没有有对应的含氧酸,故D错误;
故选:C.
点评:本题考查结构性质与位置关系、元素周期律等,题目难度不大,推断元素是解题的关键.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
下列说法正确的是( )
| A、在铁片上镀铜时,若阴极增重3.2g,则电镀液中通过的电子的物质的量为0.1mol |
| B、钢铁电化学腐蚀的两种类型主要区别在于水膜的PH不同,引起的负极反应不同 |
| C、参加反应的物质的性质是决定化学反应速率的重要因素 |
| D、电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极区产生的Cl2进入阳极区 |
下列物质互为同分异构体的一组是( )
| A、35Cl和37Cl |
| B、CH3CH2OH和CH3OCH3 |
| C、O2和O3 |
| D、甲苯和邻二甲苯 |
需要加入适当的氧化剂才能实现的反应( )
| A、SO3→HSO4- |
| B、MnO4-→Mn2+ |
| C、PCl3→PCl5 |
| D、CO2→H2CO3 |
aXm+、bYn+、cZm-、dQn-(m>n)的电子层结构相同,下列说法正确的是( )
| A、原子半径的大小顺序为:X>Y>Z>Q |
| B、离子半径的大小顺序为:Xm+>Yn+>Zm->Qn- |
| C、m+a=d-n |
| D、b-n=c+m |
下列说法正确的是( )
①NO2气体通入FeSO4溶液中无现象;
②SiC俗称金刚砂,可用作砂纸、砂轮的磨料;
③将过量CO2气体通入水玻璃溶液中可以看到有白色胶状沉淀生成;
④用铜片在加热的条件下就可鉴别浓硫酸和稀硫酸;
⑤将盛有10mlNO2和O2的混和气体的试管倒扣于水槽中一段时间后水面可能充满整个试管;
⑥70mL的H2S和90mL的O2混合点燃后恢复到原状况可产生70mL的SO2.
①NO2气体通入FeSO4溶液中无现象;
②SiC俗称金刚砂,可用作砂纸、砂轮的磨料;
③将过量CO2气体通入水玻璃溶液中可以看到有白色胶状沉淀生成;
④用铜片在加热的条件下就可鉴别浓硫酸和稀硫酸;
⑤将盛有10mlNO2和O2的混和气体的试管倒扣于水槽中一段时间后水面可能充满整个试管;
⑥70mL的H2S和90mL的O2混合点燃后恢复到原状况可产生70mL的SO2.
| A、①③④⑤ | B、②③④⑥ |
| C、①②⑥ | D、②③④⑤ |
下列说法中不正确的是( )
| A、在非标准状况下,1 mol O2的体积也有可能是22.4 L |
| B、在温度和压强一定时,气态物质的体积主要由气体分子数目和分子的大小决定 |
| C、同温同压下,0.3 mol N2和0.7 mol O2的体积比为3:7 |
| D、同温同压下,相同体积的任何气体所含有的分子数目一定相同 |
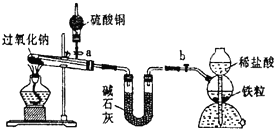 Na2O2是中学化学常用的强氧化剂,除了能与C02、H20反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况,设计了如图所示装置进行有关实验.
Na2O2是中学化学常用的强氧化剂,除了能与C02、H20反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况,设计了如图所示装置进行有关实验.