题目内容
【题目】已知X、Y、Z、W均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物已略)。下列说法不正确的是
![]()
A. X、Y、Z中至少有一种相同的元素,该元素可以是金属元素也可以是非金属元素
B. 物质W可能是化合物,也可能是单质
C. 上述转化关系中不可能出现置换反应
D. 若X、Y、Z中均含有一种常见金属元素,则W可能是强酸也可能是强碱
【答案】C
【解析】
X、Y、Z、W可以分别为①NaOH、Na2CO3、NaHCO3和CO2;②AlCl3、Al(OH)3、NaAlO2和NaOH,③NaAlO2、Al(OH)3、AlCl3和HCl,④H2S、S、SO2和O2,⑤Cl2、FeCl3、FeCl2和Fe等,故A、B、D项均正确。若为上述中的第④种情况,X→Y的转化为2H2S+O2=2S+2H2O,属于置换反应,故C项错误。

【题目】分类是学习化学的一种重要思想,下列关于物质的分类组合正确的是( )
分类组合 | 酸 | 碱 | 盐 | 酸性氧化物 | 碱性氧化物 |
A | 盐酸 | Na2CO3 | K2CO3 | CO2 | CaO |
B | 硝酸 | Ca(OH)2 | NaHSO4 | MgO | CO |
C | 硫酸 | 烧碱 | NaHCO3 | P2O5 | Na2O |
D | H2CO3 | Na2CO3 | CaCO3 | SO2 | CuO |
A. A B. B C. C D. D
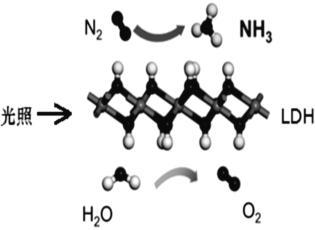
【题目】(1)工业上氨气的催化氧化反应的化学方程式_____________
(2)偏铝酸钠溶液中通入过量二氧化碳的离子方程式_____________;
(3)根据部分键能数据,以及热化学方程式CH4(g)+4F2(g) = CF4(g)+4HF(g)
ΔH =-1940 kJ·mol-1,计算H—F键的键能为______________。
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | ? | 155 |
(4)0.1mol的氯气和焦炭、TiO2固体完全反应,生成TiCl4液体和一种还原性的气体,放出热量4.28kJ,写出该反应的热化学方程式_________________。
【题目】在恒温、恒容条件下发生下列反应:2X2O5 (g) ![]() 4XO2(g) +O2(g) △H>0,T温度下的部分实验数据为:
4XO2(g) +O2(g) △H>0,T温度下的部分实验数据为:
t/s | 0 | 50 | 100 | 150 |
c(X2O5) mol/L | 4.00 | 2.50 | 2.00 | 2.00 |
下列说法错误的是
A. T温度下的平衡数为K=64 (mol/L)3,100s时转化率为50%
B. 50s 内 X2O5分解速率为 0.03 mol/ (Ls)
C. T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则Kl>K2
D. 若只将恒容改为恒压,其它条件都不变,则平衡时X2O5的转化率和平衡常数都不变
【题目】短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21。回答下列问题:
W | X | |||
Y | Z |
(1)四种元素简单离子的半径由大到小为_______(用离子符号表达)。
(2)W的最简单氢化物的电子式为______。
(3)Y单质与Fe2O3反应能放出大量的热,常用于焊接钢轨,该反应化学方程式为:________。Y的最高价氧化物与Z的气态氢化物的水溶液反应的离子方程式:__________。
(4)向盛有3 mL鸡蛋清溶液的试管里滴入几滴W的最高价氧化物的水化物浓溶液,实验现象为_________。