题目内容
8.某气态烷烃和气态单烯烃组成的混合气体在同温同压下对氢气的相对密度为13,取标准状况下此混合气体4.48L通入足量溴水中,溴水增重2.8g,此两种烃是( )| A. | 甲烷和丙烯 | B. | 乙烷和2-丁烯 | ||
| C. | 甲烷和2-甲基丙烯 | D. | 乙烯和1-丁烯 |
分析 由混合气体是同种状况下H2密度的13倍,可知混合气体的平均摩尔质量,可确定烷烃,然后由标准状况下该混合气体4.48L,溴水增重2.8g,则计算烯烃的摩尔质量,进一步得出烯烃.
解答 解:由气态烷烃和气态单烯烃组成的混合气体是同种状况下H2密度的13倍,
则M(混合)=13×2g/mol=26g/mol,
烯烃的摩尔质量最小为28g/mol,则烷烃的摩尔质量应小于26g/mol,
所以混合气体中一定含有甲烷,
设烯烃的化学式为CnH2n,标准状况下该混合气体4.48L,溴水增重2.8g,
则n(混合)=$\frac{4.48L}{22.4L/mol}$=0.2mol,混合气体质量为0.2mol×26g/mol=5.2g,
则甲烷的质量为5.2g-2.8g=2.4g,
甲烷的物质的量为$\frac{2.4g}{16g/mol}$=0.15mol,
则烯烃的物质的量为0.2mol-0.15mol=0.05mol,
所以M(CnH2n)=$\frac{2.8g}{0.05mol}$=56g/mol,
12n+2n=56,解得n=4,
即烯烃为1-丁烯、2-丁烯或2-甲基丙烯,该混合物为甲烷与2-甲基丙烯符合,
故选C.
点评 本题考查有机物分子式计算的确定,为高频考点,把握平均摩尔质量确定一定含甲烷为解答的关键,侧重分析与计算能力的考查,注意平均值法应用及烯烃性质的应用,题目难度不大.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
19.下列有关实验操作、现象、解释和结论都正确的是( )
| 选项 | 操作 | 现象 | 解释、结论 |
| A | 长期露置于潮湿空气中的Fe粉中加入足量的稀盐酸充分反应,滴入KSCN溶液 | 溶液呈红色 | 稀盐酸将Fe氧化为Fe3+ |
| B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了Na2CO3晶体 |
| C | Al箔插入浓硝酸中 | 无现象 | Al在浓硝酸中钝化,形成致密的氧化膜 |
| D | 用玻璃棒蘸取浓氨水点到蓝色石蕊试纸上 | 试纸变红色 | 浓氨水呈碱性 |
| A. | A | B. | B | C. | C | D. | D |
16.元素周期律揭示了元素间的递变规律,下列递变规律正确的是( )
| A. | ⅣA族元素氢化物沸点:SiH4>CH4,所以ⅤA族元素氢化物沸点:PH3>NH3 | |
| B. | 第二周期元素氢化物稳定性:HF>H2O,第三周期元素氢化物稳定性:HCl>H2S | |
| C. | ⅦA族元素的非金属性:F>Cl,所以ⅦA族元素氢化物的酸性:HF<HCl | |
| D. | 镁比铝活泼,工业上用电解熔融氧化铝制铝,所以工业上也用电解熔融氧化镁制镁 |
3.为了分离提纯蛋白质,不可在蛋白质溶液中加入下列试剂中的( )
| A. | 甲醛溶液 | B. | 饱和硫酸钠溶液 | C. | 硝酸铅溶液 | D. | 饱和硫酸铜溶液 |
13.下列有机物的命名正确的是( )
| A. | 二溴乙烷:CH2BrCH2Br | B. | 3-乙基-1-丁烯: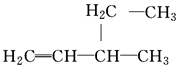 | ||
| C. | 2-甲基-2,4-己二烯: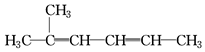 | D. | 2,2,3-三甲基戊烷: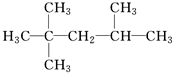 |
18. 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的两种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的两种方法:
方法a:用炭粉在高温条件下还原CuO
方法b:电解法,反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑
(1)已知:①2Cu(s)+$\frac{1}{2}$O2(g)═Cu2O(s)△H=-169kJ/mol
②C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5kJ/mol
③Cu(s)+$\frac{1}{2}$O2(g)═CuO(s)△H=-157kJ/mol
则方法a中反应的热化学方程式是:C(s)+2CuO (s)=CuO(s)+CO(g)△H=+34.5kJ/mol.
(2)方法b是用肼燃料电池为电源,通过离子交换膜电解法控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示:
①上述装置中B电极应连D电极(填“C”或“D”)
②该离子交换膜为阴离子交换膜(填“阴”或“阳”),该电解池的阳极反应式为:2Cu-2e-+2OH-=Cu2O+H2O.
③原电池中负极反应式为:N2H4-4e-+4OH-=N2↑+4H2O.
(3)在相同体积的恒容密闭容器中,用以上方法制得的两种Cu2O分别进行催化分解水的实验:
2H2O$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H>0
水蒸气的浓度随时间t变化如表所示:
①催化剂的效率:实验①<实验②(填“>”或“<”);
②实验①、②、③的化学平衡常数K1、K2、K3的大小关系为:K1=K2<K3.
 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的两种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的两种方法:方法a:用炭粉在高温条件下还原CuO
方法b:电解法,反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑
(1)已知:①2Cu(s)+$\frac{1}{2}$O2(g)═Cu2O(s)△H=-169kJ/mol
②C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5kJ/mol
③Cu(s)+$\frac{1}{2}$O2(g)═CuO(s)△H=-157kJ/mol
则方法a中反应的热化学方程式是:C(s)+2CuO (s)=CuO(s)+CO(g)△H=+34.5kJ/mol.
(2)方法b是用肼燃料电池为电源,通过离子交换膜电解法控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示:
①上述装置中B电极应连D电极(填“C”或“D”)
②该离子交换膜为阴离子交换膜(填“阴”或“阳”),该电解池的阳极反应式为:2Cu-2e-+2OH-=Cu2O+H2O.
③原电池中负极反应式为:N2H4-4e-+4OH-=N2↑+4H2O.
(3)在相同体积的恒容密闭容器中,用以上方法制得的两种Cu2O分别进行催化分解水的实验:
2H2O$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H>0
水蒸气的浓度随时间t变化如表所示:
| 号 |  | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
②实验①、②、③的化学平衡常数K1、K2、K3的大小关系为:K1=K2<K3.
 第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量.图是部分元素原子的第一电离能I1随原子序数变化的曲线图.
第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量.图是部分元素原子的第一电离能I1随原子序数变化的曲线图.