题目内容
10.下列关于水的电离叙述正确的是( )| A. | 无论在什么条件下,c(H+)增大,酸性都增强 | |
| B. | 稀释氯化铵溶液,水的电离程度变大 | |
| C. | 稀释氢氧化钠溶液,水的电离程度变小 | |
| D. | 升高温度,KW变大,H+浓度增大 |
分析 A.c(H+)增大,酸性不一定增强;
B.NH4Cl溶液,加蒸馏水稀释,其浓度减小,对水的电离的促进程度减小;
C.稀释氢氧化钠溶液,c(NaOH)减小,碱的浓度越大水的电离程度越小;
D.水的电离是吸热反应,升高温度促进水电离.
解答 解:A.c(H+)增大,酸性不一定增强,升高温度促进纯水电离,溶液中c(H+)增大但溶液仍然呈中性,故A错误;
B.NH4Cl溶液,加蒸馏水稀释,其浓度减小,对水的电离的促进程度减小,所以水的电离程度减小,故B错误;
C.稀释氢氧化钠溶液,c(NaOH)减小,碱的浓度越大水的电离程度越小,所以稀释氢氧化钠溶液,水的电离程度变大,故C错误;
D.水的电离是吸热反应,升高温度促进水电离,KW变大,H+浓度增大,故D正确;
故选D.
点评 本题以水电离为载体考查弱电解质的电离,为高频考点,明确水电离影响因素及溶液酸碱性判断方法是解本题关键,注意不能根据溶液中c(H+)大小判断溶液酸碱性,要根据溶液中c(H+)、c(OH-)相对大小判断溶液酸碱性,易错选项是A.

练习册系列答案
相关题目
5.在通常情况下,稀有气体很难与其他元素发生化学反应,其原因是( )
| A. | 稀有气体最外层电子数均为8个,很稳定 | |
| B. | 稀有气体的电子层数比较多,很稳定 | |
| C. | 稀有气体的最外层电子数均达到稳定结构 | |
| D. | 稀有气体的原子核所带电荷较多 |
15.分子式为C2H402且可与Na0H溶液反应的有机化合物有( )
| A. | 5种 | B. | 6种 | C. | 2种 | D. | 8种 |
15.在无土裁培中,配制1L含0.5mol NH4Cl、0.16mol KCl、0.24mol K2SO4的某营养液,若用KCl、NH4Cl和(NH4)2SO4三种固体配制,则需此三种固体的物质的量分别为( )
| A. | 0.40mol 0.50mol 0.12mol | B. | 0.66mol 0.50mol 0.24mol | ||
| C. | 0.64mol 0.50mol 0.24mol | D. | 0.64mol 0.02mol 0.24mol |

 ,
,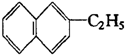 属于萘的同系物,则萘和萘的同系物分子组成通式为CnH2n-12 (n≥10).
属于萘的同系物,则萘和萘的同系物分子组成通式为CnH2n-12 (n≥10). ②丙的结构简式为
②丙的结构简式为 .
.