题目内容
12.25℃时,pH=a的X体积的某强酸与pH=b的Y体积的某强碱混合,溶液呈中性,已知a+b=15,则X:Y=10:1.分析 25℃时,pH=a的X体积的某强酸中c(H+)=10-amol/L,pH=b的强碱溶液中c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-b}}$mol/L,混合溶液呈中性,则10-a mol/L×XL=$\frac{1{0}^{-14}}{1{0}^{-b}}$mol/L×YL,a+b=15,据此计算X:Y之比.
解答 解:25℃时,pH=a的X体积的某强酸中c(H+)=10-a mol/L,pH=b的强碱溶液中c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-b}}$mol/L,混合溶液呈中性,则10-a mol/L×XL=$\frac{1{0}^{-14}}{1{0}^{-b}}$mol/L×YL,a+b=15,10 14-a-b=$\frac{Y}{X}$,X:Y=10:1,
故答案为:10:1.
点评 本题考查酸碱中和溶液定性判断,为高频考点,明确混合溶液酸碱性及pH计算方法是解本题关键,题目难度不大.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
2.下列离子方程式书写正确的是( )
| A. | FeCl2溶液中通入Cl2:Fe2++Cl2=Fe3++2Cl- | |
| B. | 澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O | |
| C. | 金属铝溶于氢氧化钠溶液 Al+2OH-=AlO2-+H2↑ | |
| D. | AlCl3溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O |
3.下列化学方程式或相应的描述涉及的反应与相应的反应类型不一致的是( )
| A. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O 氧化反应 | |
| B. | 苯中加入溴水,充分振荡静置,溴水褪色 取代反应 | |
| C. | nCH2═CHCl$\stackrel{催化剂}{→}$ 加聚反应 加聚反应 | |
| D. | CH2═CH2+Br2→CH2BrCH2Br 加成反应 |
20.只用一种试剂来鉴别碳酸钠、亚硫酸钠、硫酸钠,这种试剂可以是( )
| A. | BaCl2 | B. | 溴水 | C. | 稀盐酸 | D. | 品红溶液 |
7.工业制氢气的一个重要反应是:CO(g)+H2O(g)?CO2(g)+H2(g).已知在25℃时:
C(石墨)+$\frac{1}{2}$O2(g)═CO(g)△H=-111kJ/mol
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242kJ/mol
C(石墨)+O2(g)═CO2(g)△H=-394kJ/mol
则25℃时1mol CO与水蒸气作用转化为氢气和二氧化碳反应△H为( )
C(石墨)+$\frac{1}{2}$O2(g)═CO(g)△H=-111kJ/mol
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242kJ/mol
C(石墨)+O2(g)═CO2(g)△H=-394kJ/mol
则25℃时1mol CO与水蒸气作用转化为氢气和二氧化碳反应△H为( )
| A. | +41.kJ/mol | B. | -41kJ/mol | C. | 283kJ/mol | D. | -131kJ/mol |
4.化学实验室所用的药品,在使用时,一定要严格遵照有关规定和操作规程,保证安全.如果不慎碰倒酒精灯,洒出的酒精在桌上燃烧起来,你采取的应急措施是( )
| A. | 拨打火警电话119 | B. | 用湿抹布扑盖 | ||
| C. | 找老师一起想办法 | D. | 逃跑 |
2.如图是某含C、H、O、N四种元素的有机分子的球棍模型.下列有关该有机物的说法错误的是( )
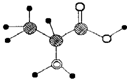

| A. | 其结构简式为:CH3CH(NH2)COOH | |
| B. | 该有机物含有两种官能团 | |
| C. | 该有机物的核磁共振氢谱显示7个吸收峰 | |
| D. | 该有机物能跟NaHCO3溶液反应产生CO2气体 |