题目内容
4.下列各物质都属于极性分子的一组是( )| A. | HF、NH3、CO、H2S | B. | NO、SO2、CCl4、H2O2 | ||
| C. | SO3、H2O、N2、SiF4 | D. | CO、BF3、CS2、PCl3 |
分析 由同种原子构成的共价键是非极性键,不同原子构成的共价键是极性键;分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,这样的分子为极性分子,以极性键结合的双原子一定为极性分子,以极性键结合的多原子分子如结构对称,正负电荷的重心重合,电荷分布均匀,则为非极性分子,以此来解答.
解答 解:A.HF、CO均为直线结构,不对称,均为极性分子;NH3为三角锥型、H2S为V型,结构不对称,均为极性分子,故A选;
B.CCl4为正四面体结构,结构对称,正负电荷的重心重合,电荷分布均匀,则为非极性分子,其它为极性分子,故B不选;
C.SO3(平面三角形)、N2(直线形)、SiF4(正四面体结构)均为非极性分子,H2O为V型,为极性分子,故C不选;
D.BF3(平面三角形)、CS2(直线形)为非极性分子,CO、PCl3为极性分子,故D不选;
故选A.
点评 本题考查化学键、分子空间构型及分子极性等,为高频考点,把握常见物质的结构、结构是否对称为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
15.下图是用辉铜矿和软锰矿制备硫酸锰和碱式碳酸铜的工艺流程:
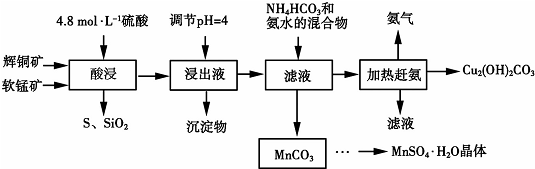
已知:①部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):
②[Cu(NH3)4]S04常温稳定,在热水溶液中会分解生成NH3
③MnO2有较强的氧化性,能将金属硫化物中的硫氧化为单质硫
④辉铜矿主要成分为Cu2S,此外还含有少量SiO2、Fe2O3等杂质,软锰矿主要含有MnO2,另外含少量SiO2、Fe2O3等杂质.
(1)实验室需要220mL 4.8mol.L-1的稀硫酸,配制时所需的玻璃仪器除烧杯、量筒、玻
璃棒外还需要250mL容量瓶、胶头滴管.
(2)酸浸时,得到的浸出液中主要含有Cu2+、Mn2+等.写出该反应的化学方程式:2MnO2+Cu2S+4H2SO4=S+2CuSO4+2MnSO4+4H2O.酸浸时,为了提高浸取率可采取的措施有粉碎矿石(或适当升高温度或搅拌)(任写两点).
(3)浸出液的pH调至4时,所得主要沉淀物的化学式为Fe(OH)3.
(4)该工艺流程中可循环使用的物质是NH3 (写化学式).
(5)用标准的BaCl2溶液测定样品中MnSO4•H2O的质量分数时,发现样品纯度大于100%(测定过程中产生的误差可忽略),其可能的原因有混有硫酸盐杂质或部分晶体失去结晶水(任写一种).

已知:①部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):
| 物质 | Cu(OH)2 | Fe(OH)2 | Mn(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 8.3 | 1.4 |
| 沉淀完全pH | 13 | 14 | 9.8 | 3.7 |
③MnO2有较强的氧化性,能将金属硫化物中的硫氧化为单质硫
④辉铜矿主要成分为Cu2S,此外还含有少量SiO2、Fe2O3等杂质,软锰矿主要含有MnO2,另外含少量SiO2、Fe2O3等杂质.
(1)实验室需要220mL 4.8mol.L-1的稀硫酸,配制时所需的玻璃仪器除烧杯、量筒、玻
璃棒外还需要250mL容量瓶、胶头滴管.
(2)酸浸时,得到的浸出液中主要含有Cu2+、Mn2+等.写出该反应的化学方程式:2MnO2+Cu2S+4H2SO4=S+2CuSO4+2MnSO4+4H2O.酸浸时,为了提高浸取率可采取的措施有粉碎矿石(或适当升高温度或搅拌)(任写两点).
(3)浸出液的pH调至4时,所得主要沉淀物的化学式为Fe(OH)3.
(4)该工艺流程中可循环使用的物质是NH3 (写化学式).
(5)用标准的BaCl2溶液测定样品中MnSO4•H2O的质量分数时,发现样品纯度大于100%(测定过程中产生的误差可忽略),其可能的原因有混有硫酸盐杂质或部分晶体失去结晶水(任写一种).
12.下列烃在光照下与氯气反应,只生成一种一氯代物的有( )
| A. | 2-甲基丙烷 | B. | 正戊烷 | C. | 2,2-二甲基丁烷 | D. | 2,2-二甲基丙烷 |
19.用硫酸酸化的CrO3遇酒精后,其颜色会从红色变为蓝绿色,用这个现象可以判断汽车司机是否酒后驾车.反应的化学方程式如下:2CrO3+3C2H5OH+3H2SO4═Cr2(SO4)3+3CH3CHO+6H2O
下列有关说法正确的是( )
下列有关说法正确的是( )
| A. | C2H5OH是氧化剂 | B. | C2H5OH发生氧化反应 | ||
| C. | CrO3是还原剂 | D. | H2SO4是氧化剂 |
16.按官能团分类,下列说法不正确的是( )
| A. | 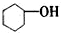 属于醇类 属于醇类 | B. |  属于羧酸 属于羧酸 | C. | 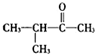 属于酮类 属于酮类 | D. |  属于酚类 属于酚类 |
13.下列说法中正确的( )
| A. | 漂白粉是纯净物,漂白液是混合物 | |
| B. | 漂白粉中含有次氯酸,所以漂白粉能使燃料等有机色素褪色 | |
| C. | 工业上将氯气通入澄清石灰水制取漂白粉 | |
| D. | 次氯酸能杀死病菌,所以氯气可用于自来水的消毒 |