题目内容
【题目】某溶液中可能含有下列6种离子中的某几种:Cl、SO42—、NH4+、CO32—、K+、Na+。为确认溶液组成进行如下实验:
①200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30 g,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶。
②向①的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12 L(已换算成标准状况,假定产生的气体全部逸出)。
(1)溶液一定存在的离子有____,可能存在的离子有______;
(2)原溶液中c(CO32—)为____,c(NH4+)____c(SO42—) (填“>、<或=”);
(3)如果上述6种离子都存在,则c(Cl)__c(SO42—) (填“>、<或=”)。
【答案】CO32—、SO42—、NH4+ Cl、K+、Na+0.05 mol/L>>
【解析】
①取少量该溶液加入BaCl2溶液有白色沉淀生成,再加入足量盐酸后,沉淀部分溶解,并有气体生成,说明白色沉淀为BaCO3和BaSO4,质量一共是4.3 g,则溶液中含有![]() 、
、![]() ,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶,则硫酸钡的质量是2.33 g,所以硫酸根离子的物质的量是
,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶,则硫酸钡的质量是2.33 g,所以硫酸根离子的物质的量是![]() ="0.01" mol,所以碳酸钡的质量是4.3 g2.33 g="1.97" g,
="0.01" mol,所以碳酸钡的质量是4.3 g2.33 g="1.97" g,![]() 的物质的量是
的物质的量是![]() ="0.01" mol;②向①的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体是氨气,物质的量是
="0.01" mol;②向①的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体是氨气,物质的量是![]() ="0.05" mol,说明溶液中有
="0.05" mol,说明溶液中有![]() 的物质的量是0.05 mol;综合以上
的物质的量是0.05 mol;综合以上
(1)溶液一定存在的离子有:![]() 、
、![]() 、
、![]() ;可能存在的离子有:Cl、K+、Na+。
;可能存在的离子有:Cl、K+、Na+。
(2)依据计算得出c(![]() )=
)=![]() ="0.05" mol/L,
="0.05" mol/L,![]() 为0.01 mol,
为0.01 mol,![]() 为0.05 mol,故c(
为0.05 mol,故c(![]() )>c(
)>c(![]() )。
)。
(3)依据溶液电中性原则,假设都存在,那么0.05 mol+n(Na+)+n(K+)="2×0.01" mol+2×0.01 mol+n(Cl),据此得出n(Cl)=n(Na+)+n(K+)+0.01 mol>0.01 mol。

【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl22H2O的流程如下:
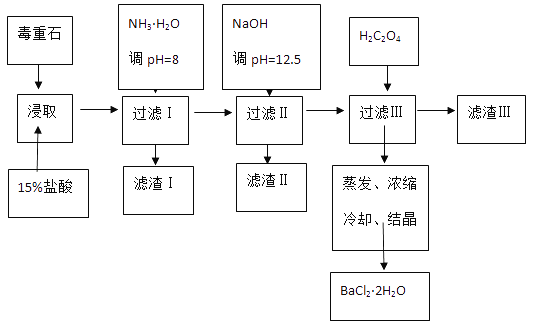
(1)实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的_________。
a.烧杯 b.容量瓶 c.玻璃棒 d.滴定管
(2)加入NH3H2O调节pH=8可除去_______(填离子符号),滤渣Ⅱ中含________(填化学式)。加入H2C2O4时应避免过量,原因是___________。
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
向BaC2O4悬浊液中加入CaCl2,可发生沉淀的部分转化,请写出反应过程中的离子方程式___________________,计算该反应的平衡常数K=___________(Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9,保留一位小数)
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。已知:2CrO42-+2H+=Cr2O72-+H2O Ba2++CrO42-=BaCrO4↓
步骤Ⅰ:移动x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b molL-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL。
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b molL-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。根据上述数据,可计算出BaCl2溶液浓度为_________molL-1(用含字母的式子表示)。若步骤Ⅱ中滴加盐酸时有少量待测液溅出,则Ba2+浓度的测量值将_______(填“偏大”或“偏小”)。