题目内容
【题目】在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,下列叙述中不正确的是( )
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,下列叙述中不正确的是( )
A.x的值为2
B.A的转化率为60%
C.B的平衡浓度为0.8 mol/L
D.D的体积分数为25%
【答案】D
【解析】
3A(g) | B(g) | xC(g) | 2D(g) | |
起始(mol) | 1 | 1 | 0 | 0 |
转化(mol) | 0.6 | 0.2 | 0.2x | 0.4 |
平衡(mol) | 0.4 | 0.8 | 0.2x | 0.4 |
A、根据平衡时C的浓度可知,x=2,A不符合题意;
B、由转化率的定义等,A的转化率为60%,B不符合题意;
C、根据三段式可知平衡时,B的平衡浓度为0.8 mol/L,C不符合题意;
D、D的体积分数为: ![]() ,D不符合题意。
,D不符合题意。
答案为D
【考点精析】利用化学反应速率的概念和反应速率的定量表示方法对题目进行判断即可得到答案,需要熟知化学反应速率是用来衡量化学反应进行快慢程度的,通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示;反应速率的单位:mol/(L·min)或mol/(L·s) v=△c-△t.

【题目】NO2为红棕色气体,可在火箭燃料中作氧化剂。回答下列问题:
(1)火箭用N2H4和NO2作燃料,产物绿色无污染,该反应的化学方程式为____________。
(2)为探究NO2和铁粉反应的产物,某小组按下图所示装置进行实验。
已知:①二者反应可能的还原产物为N2或NO
②沸点:NO2(21℃),NO(-152℃)
③酸性KMnO4溶液能氧化NO生成NO3-
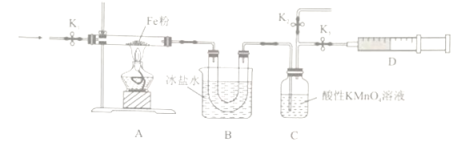
①按上图所示组装完实验仪器后,下一步操作为______________________________。
②实验前需利用气体X将装置的空气排净,气体X可以为_______(填标号)。
A.Ar B.H2 C.CO D.NO2
③排净空气后,后续实验的最佳操作顺序是___c、b(填标号)。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.打开K1和K2,关闭K3,缓缓通入气体X
d.打开K1和K3,关闭K2,缓缓通入NO2 e.关闭K1,停止通入NO2
④装置B的作用是__________________________________。
(3)分析NO2和铁粉反应的产物
①实验过程中A、C装置的物质均无明显颜色变化,D收集到无色气体。由此可推知气体产物为____________________________。
②取少量固体产物于试管,先加入盐酸充分溶解,再加入KSCN溶液,溶液若无血红色,则产物不含三价铁。该方案是否可行并说明理由:_______________________________。
③实验得到的相关数据如下表:
玻璃管质量/g | Fe质量/g | 反应后(玻璃管+固体)/g |
m | 1.12 | m+1.52 |
综合实验现象和计算可知,固体生成物一定有______(填“FeO”Fe2O3”或“Fe3O4”);反应的方程式为______