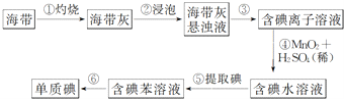
��Ŀ����
����Ŀ��NO2Ϊ����ɫ���壬���ڻ��ȼ���������������ش���������:
(1)�����N2H4��NO2��ȼ�ϣ�������ɫ����Ⱦ���÷�Ӧ�Ļ�ѧ����ʽΪ____________��
(2)Ϊ̽��NO2�����۷�Ӧ�IJ��ijС�鰴��ͼ��ʾװ�ý���ʵ�顣
��֪:�ٶ��߷�Ӧ���ܵĻ�ԭ����ΪN2��NO
�ڷе�:NO2(21��)��NO(-152��)
������KMnO4��Һ������NO����NO3-
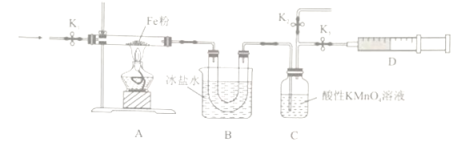
�ٰ���ͼ��ʾ��װ��ʵ����������һ������Ϊ______________________________��
��ʵ��ǰ����������X��װ�õĿ����ž�������X����Ϊ_______(����)��
A.Ar B.H2 C.CO D.NO2
���ž���������ʵ�����Ѳ���˳����___c��b(����)��
a.��ȼ�ƾ��ƣ����� b.Ϩ��ƾ��� c.��K1��K2���ر�K3������ͨ������X
d.��K1��K3���ر�K2������ͨ��NO2 e.�ر�K1��ֹͣͨ��NO2
��װ��B��������__________________________________��
(3)����NO2�����۷�Ӧ�IJ���
��ʵ�������A��Cװ�õ����ʾ���������ɫ�仯��D�ռ�����ɫ���塣�ɴ˿���֪�������Ϊ____________________________��
��ȡ��������������Թܣ��ȼ����������ܽ⣬�ټ���KSCN��Һ����Һ����Ѫ��ɫ������ﲻ�����������÷����Ƿ���в�˵������:_______________________________��
��ʵ��õ�������������±�:
����������/g | Fe����/g | ��Ӧ��(������+����)/g |
m | 1.12 | m+1.52 |
�ۺ�ʵ������ͼ����֪������������һ����______(�FeO��Fe2O3����Fe3O4��)����Ӧ�ķ���ʽΪ______
���𰸡�2NO2 + 2N2H4 ![]() 3N2 + 4H2O ���װ��������Aade��δ��Ӧ�� NO2 ��ȴN2�����ڹ�����������Һ�е�������ȫ����ԭ����ҺҲ��Ѫ��ɫFe3O43Fe+2NO2
3N2 + 4H2O ���װ��������Aade��δ��Ӧ�� NO2 ��ȴN2�����ڹ�����������Һ�е�������ȫ����ԭ����ҺҲ��Ѫ��ɫFe3O43Fe+2NO2 ![]() Fe3O4+N2
Fe3O4+N2
��������
���⿼����ǵ��Ļ���������ʣ�����ʵ��ԭ���ǹؼ���
(1) N2H4��NO2��Ӧ������ɫ����Ⱦ�IJ��Ϊ������ˮ������ʽΪ��2NO2 + 2N2H4 ![]() 3N2 + 4H2O�� (2) ����װ��������Ӧ�Ƚ��м��װ�������ԣ��� Ҫ̽���������������ķ�Ӧ����������������������˲���ʹ��������һ����̼�Ȼ�ԭ�����壬������ʹ�ö�����������ѡA�����ž�������ȼ�ƾ��ƣ����ȣ�Ȼ��K1��K3���ر�K2������ͨ��NO2����Ȼ��ر�K1��ֹͣͨ�����������Ȼ����ͨ������X������������ϵ����Ը��������Һ����ӳ����˳��Ϊ��adecb���ܶ�����������Һ���������ñ�ˮ��δ��Ӧ�� NO2 ��ȴ���Է��룻(3) ��A��Cװ�õ����ʾ���������ɫ�仯��˵��û������һ��������D���ռ�����ɫ���壬˵������ΪN2���������ڹ�����������Һ�е�������ȫ����ԭ����ҺҲ��Ѫ��ɫ�����Բ���˵�������в�������������Ϊ��Ӧǰ��������ɫû�б仯���ų����������ɵĿ����ԣ���Ӧ���������Ϊ1.52-1.12=0.40�ˣ�Ϊ��Ԫ�ص��������������ʵ���Ϊ1.12/56=0.02mol����Ԫ�ض����ʵ���Ϊ0.4/16=0.025mol��������ԭ�����ʵ�����Ϊ0.02��0.025=4:5��˵����������������������ʽΪ�� 3Fe+2NO2
3N2 + 4H2O�� (2) ����װ��������Ӧ�Ƚ��м��װ�������ԣ��� Ҫ̽���������������ķ�Ӧ����������������������˲���ʹ��������һ����̼�Ȼ�ԭ�����壬������ʹ�ö�����������ѡA�����ž�������ȼ�ƾ��ƣ����ȣ�Ȼ��K1��K3���ر�K2������ͨ��NO2����Ȼ��ر�K1��ֹͣͨ�����������Ȼ����ͨ������X������������ϵ����Ը��������Һ����ӳ����˳��Ϊ��adecb���ܶ�����������Һ���������ñ�ˮ��δ��Ӧ�� NO2 ��ȴ���Է��룻(3) ��A��Cװ�õ����ʾ���������ɫ�仯��˵��û������һ��������D���ռ�����ɫ���壬˵������ΪN2���������ڹ�����������Һ�е�������ȫ����ԭ����ҺҲ��Ѫ��ɫ�����Բ���˵�������в�������������Ϊ��Ӧǰ��������ɫû�б仯���ų����������ɵĿ����ԣ���Ӧ���������Ϊ1.52-1.12=0.40�ˣ�Ϊ��Ԫ�ص��������������ʵ���Ϊ1.12/56=0.02mol����Ԫ�ض����ʵ���Ϊ0.4/16=0.025mol��������ԭ�����ʵ�����Ϊ0.02��0.025=4:5��˵����������������������ʽΪ�� 3Fe+2NO2 ![]() Fe3O4+N2��
Fe3O4+N2��