题目内容
13.无色溶液X由Na+、Ag+、Ba2+、Al3+、AlO2-、MnO4-、CO32-、SO42-中的若干种离子组成,取溶液进行如下连续实验: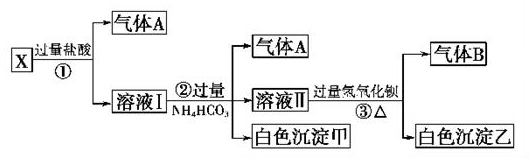
(1)气体A的成分是(填化学式,下同)CO2,气体B的成分是:NH3.
(2)溶液中一定存在的离子有:Na+、AlO2-、CO32-,可能存在的离子有:SO42-.
分析 溶液为无色,可知不存在高锰酸根离子,加入盐酸生成气体,可知一定含有碳酸根离子,排除银离子、钡离子、铝离子,溶液呈电中性,所以一定含有阳离子钠离子,溶液I加入过量碳酸氢铵反应生成二氧化碳,白色沉淀甲是偏铝酸根离子和过量盐酸反应生成的铝离子与碳酸根或碳酸氢根水解生成的氢氧化铝沉淀,判断原溶液一定含有AlO2-;溶液Ⅱ加入过量氢氧化钡生成气体B为NH3,沉淀乙为碳酸钡沉淀或碳酸钡和硫酸钡沉淀的混合物,以此解答该题.
解答 解:(1)溶液X是无色的,所以一定没有MnO4-.加入盐酸能生成气体,则根据离子的种类可知,一定含有CO32-,因此一定不存在Ag+、Ba2+、Al3+,气体A是CO2.溶液Ⅱ中含有NH4+,能和强碱反应生成氨气,即B是氨气,
故答案为:CO2;NH3;
(2)由于溶液I能和碳酸氢铵反应生成白色沉淀,所以原溶液中一定含有AlO2-,和盐酸反应生成铝离子,进而和碳酸氢铵反应生成氢氧化铝白色沉淀.根据电荷守恒定律可知,一定含有钠离子,所以原溶液中含有的离子是Na+、AlO2-、CO32-.由于溶液Ⅱ中HCO3-,也能和氢氧化钡反应生成碳酸钡白色沉淀,即乙不一定是硫酸钡沉淀,所以原溶液中的SO42-不能确定,
故答案为:Na+、AlO2-、CO32-;SO42-.
点评 本题为离子推断题,为高频考点,侧重于学生的分析能力和实验能力的考查,明确物质的特殊性质及相互转化关系是解题关键,注意盐类的双水解的反应,题目难度中等.

练习册系列答案
相关题目
3.CO(g)+H2O(g)═H2(g)+CO2(g)△H<0,在其他条件不变的情况下( )
| A. | 加入催化剂,改变了反应的途径,反应的△H也随之改变 | |
| B. | 反应物总能量小于生成物总能量 | |
| C. | 若在原电池中进行,反应放出的热量不变 | |
| D. | 升高温度,反应速率加快,但反应的△H不变 |
4.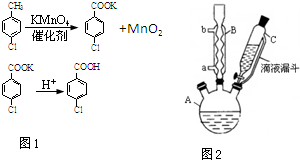 对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和农药的合成,实验室中制备对氯苯甲酸的反应(图1)、装置图如图2:
对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和农药的合成,实验室中制备对氯苯甲酸的反应(图1)、装置图如图2:
常温条件下的有关数据如下表所示:
实验步骤:在规格为250mL的装置A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩;然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量为7.19g.
请回答下列问题:
(1)装置B的名称是球形冷凝管.
(2)量取6.00mL对氯甲苯应选用的仪器是C.
A.10mL量筒 B.50mL容量瓶 C.50mL酸式滴定管 D.50mL碱式滴定管
(3)控制温度为93℃左右的方法是水浴加热.对氯甲苯的加入方法是逐滴加入而不是一次性加入,原因是减少对氯甲苯的挥发,提高原料利用率.
(4)第一次过滤的目的是除去MnO2,滤液中加入稀硫酸酸化,可观察到的实验现象产生白色沉淀.
(5)第二次过滤所得滤渣要用冷水进行洗涤,其原因是可除去对氯苯甲酸表面的可溶性杂质且尽量减小对氯苯甲酸的损耗.
(6)本实验的产率是D(填标号).
A.60% B.70% C.80% D.90%
 对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和农药的合成,实验室中制备对氯苯甲酸的反应(图1)、装置图如图2:
对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和农药的合成,实验室中制备对氯苯甲酸的反应(图1)、装置图如图2:常温条件下的有关数据如下表所示:
| 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 颜色 | 水溶性 | |
| 对氯甲苯 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
| 对氯苯甲酸 | 243 | 275 | 1.54 | 白色 | 微溶 |
| 对氯苯甲酸钾 | 具有盐的通性,属于可溶性盐 | ||||
请回答下列问题:
(1)装置B的名称是球形冷凝管.
(2)量取6.00mL对氯甲苯应选用的仪器是C.
A.10mL量筒 B.50mL容量瓶 C.50mL酸式滴定管 D.50mL碱式滴定管
(3)控制温度为93℃左右的方法是水浴加热.对氯甲苯的加入方法是逐滴加入而不是一次性加入,原因是减少对氯甲苯的挥发,提高原料利用率.
(4)第一次过滤的目的是除去MnO2,滤液中加入稀硫酸酸化,可观察到的实验现象产生白色沉淀.
(5)第二次过滤所得滤渣要用冷水进行洗涤,其原因是可除去对氯苯甲酸表面的可溶性杂质且尽量减小对氯苯甲酸的损耗.
(6)本实验的产率是D(填标号).
A.60% B.70% C.80% D.90%
1.美丽、芳香的鲜花,会给紧张而又忙碌的工作、学习、生活带来轻松和愉悦的心情.如果在花瓶中加入“鲜花保鲜剂”,就会延长鲜花的寿命.下表是1L“鲜花保鲜剂”的成分,请你阅读后回答下列问题:
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是蔗糖 .(填写名称).
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林中不含K+):2×$\frac{0.50}{174}$+$\frac{0.50}{158}$mol•L -1(只要求写表达式,不需计算).
(3)配制上述lL“鲜花保鲜剂”所需的仪器有:托盘天平、烧杯、玻璃棒、药匙、1000 mL容量瓶 、胶头滴管 .(在横线上填写所缺仪器的名称).
(4)配制过程中,下列操作配制结果没有影响的是AD(填字母).
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaC1溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,可加入的试剂中含有Cl-(填化学符号)
| 成分 | 质量(g) | 摩尔质量( mol•L -1) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林中不含K+):2×$\frac{0.50}{174}$+$\frac{0.50}{158}$mol•L -1(只要求写表达式,不需计算).
(3)配制上述lL“鲜花保鲜剂”所需的仪器有:托盘天平、烧杯、玻璃棒、药匙、1000 mL容量瓶 、胶头滴管 .(在横线上填写所缺仪器的名称).
(4)配制过程中,下列操作配制结果没有影响的是AD(填字母).
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaC1溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,可加入的试剂中含有Cl-(填化学符号)
8.有一包白色粉末,由BaCl2、K2SO4、CaCO3、NaOH、CuSO4中的一种或几种组成,为了探究它的成份,进行了如下实验:下列判断正确的是( )
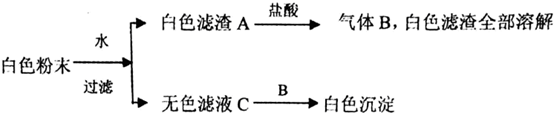

| A. | BaCl2,CaCO3一定存在,NaOH可能存在 | |
| B. | K2SO4、CuSO4一定不存在 | |
| C. | K2SO4、NaOH、CaCO3、BaCl2一定存在,K2SO4可能存在 | |
| D. | C为单一溶质溶液 |
5.某学生用托盘天平称取3.3g食盐,称量时指针若左偏,此时应该( )
| A. | 增加药品 | B. | 减少药品 | C. | 增加砝码 | D. | 减少砝码 |
2.下列各组离子,在溶液中能大量共存、加入NaOH溶液后加热既有气体放出又有沉淀生成的一组是( )
| A. | Ba2+、NO3-、NH4+、Cl- | B. | K+、Ba2+、Cl-、SO42- | ||
| C. | Al3+、CO32-、NH4+、AlO2- | D. | Cu2+、NH4+、SO42-、K+ |
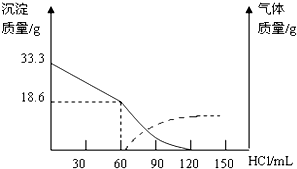
3.某天然碱(纯净物)可看作由CO2和NaOH反应后的产物所组成.称取天然碱样品四份,溶于水后,分别逐滴加入相同浓度的盐酸溶液30mL,产生CO2的体积(标准状况)如表:
(1)由第Ⅰ组数据中的CO2体积与样品质量之比,可以推测用2.49g样品进行同样的实验时,产生CO2504mL(标准状况).
(2)另取3.32g天然碱样品于300℃加热分解至完全(300℃时Na2CO3不分解),产生CO2112mL(标准状况)和水0.45g,计算并确定该天然碱的化学式.
(3)已知Na2CO3和HCl(aq)的反应分下列两步进行:
Na2CO3+HCl→NaCl+NaHCO3 Na2CO3+HCl→NaCl+CO2↑+H2O
由上表中第Ⅳ组数据可以确定所用的HCl(aq)的浓度为2.5mol/L.
(4)依据表所列数据以及天然碱的化学式,讨论并确定上述实验中CO2(标准状况)体积V(mL)与样品质量W(g)之间的关系式.
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | |
| 盐酸液的体积(mL) | 30 | 30 | 30 | 30 |
| 样品(g) | 3.32 | 4.15 | 5.81 | 7.47 |
| 二氧化碳的体积(mL) | 672 | 840 | 896 | 672 |
(2)另取3.32g天然碱样品于300℃加热分解至完全(300℃时Na2CO3不分解),产生CO2112mL(标准状况)和水0.45g,计算并确定该天然碱的化学式.
(3)已知Na2CO3和HCl(aq)的反应分下列两步进行:
Na2CO3+HCl→NaCl+NaHCO3 Na2CO3+HCl→NaCl+CO2↑+H2O
由上表中第Ⅳ组数据可以确定所用的HCl(aq)的浓度为2.5mol/L.
(4)依据表所列数据以及天然碱的化学式,讨论并确定上述实验中CO2(标准状况)体积V(mL)与样品质量W(g)之间的关系式.