题目内容
【题目】胆矾(CuSO45H2O)高温时发生反应:2CuSO45H2O![]() 2CuO + 2SO2↑+ O2↑+ 10H2O。下列装置能达到实验目的的是( )
2CuO + 2SO2↑+ O2↑+ 10H2O。下列装置能达到实验目的的是( )
A.可用于胆矾分解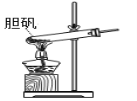
B.可用于检验产物是否含H2O 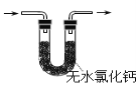
C.可用于收集O2 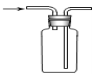
D.可用于吸收胆矾分解的SO2 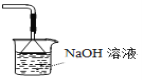
【答案】D
【解析】
根据所给反应的条件、反应物生成物的状态、性质进行分析解答。
A.固体加热试管口应略向下倾斜,A错误;
B.氯化钙吸水后没有明显现象,无法检验产物是否含水, B错误;
C.氧气的密度比空气大,应该用向上排空气法收集,从长导管一侧进气,既进气管应“长进短出”,C错误;
D.SO2能与NaOH反应,倒扣的漏斗可以防倒吸,图中装置可以用来吸收胆矾分解产生的SO2,D正确;
答案选D。

练习册系列答案
相关题目
【题目】为提纯下列物质![]() 括号内物质为杂质
括号内物质为杂质![]() ,所选用的试剂和分离方法都正确的是( )
,所选用的试剂和分离方法都正确的是( )
选项 | 物质 | 除杂试剂 | 分离方法或操作 |
A | 乙醇 | 无水 | 充分反应后蒸馏 |
B | 苯 | NaOH溶液 | 振荡静置后过滤 |
C | NaCl固体 | 水 | 高温溶解、降温结晶 |
D |
| 饱和 | 充分浸泡后过滤 |
A.AB.BC.CD.D