题目内容
一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合题图示的是( )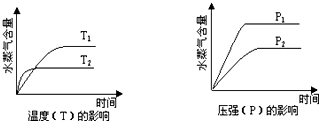

| A、CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g);△H<0 |
| B、2C6H5CH2CH3(g)+O2(g) 2C6H5CH=CH2(g)+2H2O(g);△H<0 |
| C、CH3CH2OH(g) CH2=CH2(g)+H2O(g);△H>0 |
| D、CO2(g)+H2(g) CO(g)+H2O(g);△H>0 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:由图象可以看出,随着温度的升高,水蒸气的含量减小,说明升高温度平衡向逆反应方向移动,则正反应应为放热反应,增大压强,水蒸气的含量增大,说明增大压强平衡向正反应方向移动,则气体反应物的化学计量数之和大于气体生成物的化学计量数之和,以此解答该题.
解答:
解:温度越高,反应越快,到达平衡的时间就越少,因此T2>T;同理压强越大,反应越快,到达平衡的时间就越少,因此p1>p2;
A.反应是一个体积减小的、放热的可逆反应,因此升高温度平衡向逆反应方向移动,降低水蒸气的含量;而增大压强平衡向正反应方向移动,增大水蒸气的含量,故A正确;
B.反应是一个体积增大的、放热的可逆反应,压强不符合,故B错误;
C.反应是一个体积增大的、吸热的可逆反应,升高温度平衡向正反应方向移动,增大水蒸气的含量,不符合图象,故C错误;
D.反应是一个体积不变的、吸热的可逆反应,压强对水蒸气的含量不影响;升高温度平衡向正反应方向移动,增大水蒸气的含量,因此均不符合,故D错误;
故选A.
A.反应是一个体积减小的、放热的可逆反应,因此升高温度平衡向逆反应方向移动,降低水蒸气的含量;而增大压强平衡向正反应方向移动,增大水蒸气的含量,故A正确;
B.反应是一个体积增大的、放热的可逆反应,压强不符合,故B错误;
C.反应是一个体积增大的、吸热的可逆反应,升高温度平衡向正反应方向移动,增大水蒸气的含量,不符合图象,故C错误;
D.反应是一个体积不变的、吸热的可逆反应,压强对水蒸气的含量不影响;升高温度平衡向正反应方向移动,增大水蒸气的含量,因此均不符合,故D错误;
故选A.
点评:本题考查外界条件对化学平衡的影响及有关图象的分析和识别,题目难度中等,解答本题的关键是能正确分析温度、压强对平衡移动的影响.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
用惰性电极实现电解,下列说法正确的是( )
| A、电解NaNO3溶液,在阴极上和阳极上析出产物的物质的量之比为2:1 |
| B、电解CuSO4溶液一段时间后,再加入一定质量Cu(OH)2,溶液能与原溶液完全一样 |
| C、电解硫酸钠溶液时,Na+向阳极移动 |
| D、电解KOH溶液,实质上是电解水,故溶液pH不变 |
某有机化合物的结构简式为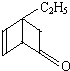 ;其中属于芳香醇的同分异构体共有( )
;其中属于芳香醇的同分异构体共有( )
 ;其中属于芳香醇的同分异构体共有( )
;其中属于芳香醇的同分异构体共有( )| A、4种 | B、5种 | C、6种 | D、8种 |
运用相关化学知识进行判断,下列结论错误的是( )
| A、可燃冰主要由甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 |
| B、增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率 |
| C、某吸热反应能自发进行,因此该反应是熵增反应 |
| D、NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 |
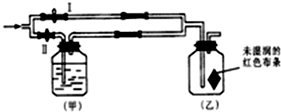
 在一定条件下,可逆反应A+B?mC变化如图所示.已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:
在一定条件下,可逆反应A+B?mC变化如图所示.已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问: