题目内容
下列关于常见有机物的说法中,正确的是( )
| A、汽油、苯、乙醇都属于烃类物质 |
| B、含5个碳原子的有机物,分子中最多可形成5个碳碳单键 |
| C、等物质的量的乙醇和乙酸完全燃烧时所需氧气的质量相等 |
| D、苯和乙烯都能使溴水褪色,二者反应原理相同 |
考点:生活中的有机化合物,有机化学反应的综合应用
专题:
分析:A、烃类物质只含碳和氢两种元素;
B、对于环状化合物,含有5个碳原子的化合物最多可以形成5个碳碳键;
C、乙醇的分子式为C2H6O,1mol乙醇完全燃烧消耗3mol氧气;乙酸的分子式为C2H4O2,1mol乙酸完全燃烧消耗2mol氧气;
D、二氧化硫和乙烯都能使溴水褪色,前者是氧化反应,后者是加成反应.
B、对于环状化合物,含有5个碳原子的化合物最多可以形成5个碳碳键;
C、乙醇的分子式为C2H6O,1mol乙醇完全燃烧消耗3mol氧气;乙酸的分子式为C2H4O2,1mol乙酸完全燃烧消耗2mol氧气;
D、二氧化硫和乙烯都能使溴水褪色,前者是氧化反应,后者是加成反应.
解答:
解:A、烃类物质只含碳和氢两种元素,乙醇属于烃的衍生物,故A错误;
B、链状化合物中,5个C最多形成4个C-C键,而对于环状化合物中,5个C最多可以形成5个C-C键,故B正确;
C、1mol乙醇完全反应消耗3mol氧气,1mol乙酸完全反应消耗2mol氧气,所以等物质的量的二者完全燃烧,消耗的氧气的质量不相等,故C错误;
D、二氧化硫和乙烯都能使溴水褪色,前者是氧化反应,后者是加成反应,反应原理不同,故D错误.
故选B.
B、链状化合物中,5个C最多形成4个C-C键,而对于环状化合物中,5个C最多可以形成5个C-C键,故B正确;
C、1mol乙醇完全反应消耗3mol氧气,1mol乙酸完全反应消耗2mol氧气,所以等物质的量的二者完全燃烧,消耗的氧气的质量不相等,故C错误;
D、二氧化硫和乙烯都能使溴水褪色,前者是氧化反应,后者是加成反应,反应原理不同,故D错误.
故选B.
点评:本题考查了常见有机物的组成结构与性质、反应原理等,题目难度中等,注意掌握常见有机物的结构与性质,注意环状化合物的特点.

练习册系列答案
相关题目
一定量Na2O2与一定量的CO2反应后的固体物质18.4g,恰好与400mL 1mol?L-1的稀盐酸完全反应,以下说法合理的是(NA表示阿伏伽德罗常数)( )
| A、反应中电子转移数为0.2NA |
| B、一定量的CO2为0.1NA |
| C、18.4 g固体物质为0.1mol Na2CO3和0.1molNa2O2的混合物 |
| D、一定量的Na2O2为0.1mol |
下列有关说法正确的是( )
| A、H7N9型禽流感是一种新型禽流感,流感病毒通常检测方法是基于核酸检测的原理.核酸一种是蛋白质 |
| B、侯德榜发明了侯氏制碱法、维勒用氮气和氢气合成了氨气、阿伦尼乌斯创立了电离学说、扫描隧道显微镜的发明和STM技术应用等等,这些都对化学学科的应用和发展作出了重要的贡献 |
| C、使用可再生资源、注重原子的经济性、推广利用二氧化碳与环氧丙烷生成的生物降解材料等都是绿色化学的内容 |
| D、化学帮助人类创造和合成了大量材料,如高纯硅制作太阳能电池、聚氯乙烯塑料用来食品包装、人造刚玉Al2O3用作耐高温材料等等 |
下列试剂用自来水配制不会导致药品变质的是( )
| A、硝酸银 | B、氯化钠 |
| C、亚硫酸钠 | D、硫代硫酸钠 |
应用元素周期律分析下列推断,其中正确的是( )
| A、酸性强弱:HClO>H2SO4>H2CO3 |
| B、热稳定性:HF>HCl>HBr |
| C、已知硒(Se)与硫同主族,其最高价氧化物对应的水化物分子式为:H2SeO3 |
| D、原子半径大小:Na>P>N |
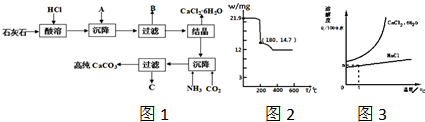
 )
)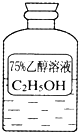 油价的持续“高烧”,引发人们对未来能源供需及价格的深切关注,并且促使人们寻求石油的替代品.
油价的持续“高烧”,引发人们对未来能源供需及价格的深切关注,并且促使人们寻求石油的替代品.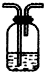

 e.
e. f.
f.
