题目内容
下列叙述正确的是( )
| A、1mol任何气体所含分子数都相等,体积也都约为22.4L |
| B、在标准状况下,18 gH2O所占的体积约是22.4L |
| C、以g?mol-1为单位时,在数值上摩尔质量与相对分子质量或相对原子质量相等 |
| D、同质量的O2和O3所含的氧原子数相同 |
考点:物质的量的相关计算
专题:计算题
分析:A.标况下气体摩尔体积是22.4L/mol,温度、压强不变,则气体摩尔体积不同;
B.标况下,水是液体,气体摩尔体积对其不适用;
C.在数值上摩尔质量与其相对分子质量或相对原子质量相等;
D.等质量的O3和O2,O原子的物质的量相同,再结合N=nNA判断氧原子数.
B.标况下,水是液体,气体摩尔体积对其不适用;
C.在数值上摩尔质量与其相对分子质量或相对原子质量相等;
D.等质量的O3和O2,O原子的物质的量相同,再结合N=nNA判断氧原子数.
解答:
解:A.气体摩尔体积受温度、压强影响,标况下气体摩尔体积是22.4L/mol,所以标况下1mol任何气体所含分子数都相等,体积也都约为22.4L,故A错误;
B.标况下,水是液体,所以气体摩尔体积对其不适用,要根据V=
计算水的体积,故B错误;
C.在数值上摩尔质量与其相对分子质量或相对原子质量相等,只是单位不同,故C错误;
D.等质量的O3和O2,O原子的物质的量相同,则由N=nNA可知,氧原子数相同,故D正确;
故选D.
B.标况下,水是液体,所以气体摩尔体积对其不适用,要根据V=
| m |
| ρ |
C.在数值上摩尔质量与其相对分子质量或相对原子质量相等,只是单位不同,故C错误;
D.等质量的O3和O2,O原子的物质的量相同,则由N=nNA可知,氧原子数相同,故D正确;
故选D.
点评:本题考查了物质的量、气体摩尔体积等知识点,注意气体摩尔体积的适用范围及适用条件,为易错点.

练习册系列答案
相关题目
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A、氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e-=4OH- |
| B、钢铁发生电化学腐蚀的负极反应式:Fe一3e-=Fe3+ |
| C、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu一2e-=Cu2+ |
| D、Pt电极电解饱和食盐水时,阳极的电极反应式为:2Cl-一2e-=Cl2↑ |
下列反应中,生成物的总焓大于反应物总焓的是( )
| A、甲烷在氧气中燃烧 |
| B、NaOH溶液与硫酸溶液混合 |
| C、硫在氧气中燃烧 |
| D、焦炭在高温下与水蒸气反应 |
天然油脂水解后的共同产物是( )
| A、硬脂酸 | B、油酸 |
| C、软脂酸 | D、甘油 |
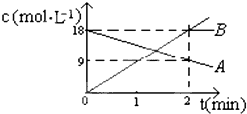 反应:A═2B中,A、B的浓度变化如图所示.则2min以内的平均反应的速率为( )
反应:A═2B中,A、B的浓度变化如图所示.则2min以内的平均反应的速率为( )| A、vA=9 mol/(L?min) |
| B、vA=4.5 mol?L?min |
| C、vB=18 mol/(L?min) |
| D、vB=9mol/(L?min) |
在无色强酸性溶液中可能大量共存的离子组是( )
| A、Ba2+、NH4+、S2-、MnO4- |
| B、NH4+、Na+、Br-、Cl- |
| C、K+、Ca2+、HSO3-、NO3- |
| D、Fe2+、NH4+、Cl-、SO32- |
常温下,发生如下反应:①16H++10Z-+2XO4-═2X2++5Z2+8H2O ②2A2++B2=2A3++2B- ③2B-+Z2=B2+2Z-
由此判断下列说法错误的是( )
由此判断下列说法错误的是( )
| A、反应Z2+2A2+=2A3++2Z-可以进行 |
| B、Z元素在反应①,③中均被还原 |
| C、氧化性由强到弱的顺序是XO4- Z2 B2 A3+ |
| D、还原性由强到弱的顺序是:A2+ B- Z- X2+ |
下列说法正确的是( )
| A、SiO2是酸性氧化物,它可以与强碱反应,不能与任何酸反应 | ||||
B、根据SiO2+Na2CO3
| ||||
| C、CO2气体通入到Na2SiO3溶液中可以制得硅酸 | ||||
| D、SiO2可以与水反应生成相对应的酸--硅酸 |
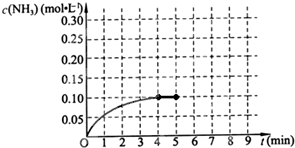 在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g);△H<0,反应中NH3的物质的量浓度的变化情况如图所示,请回答下列问题:
在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g);△H<0,反应中NH3的物质的量浓度的变化情况如图所示,请回答下列问题: