题目内容
19.下列实验方法或操作正确的是( )| A. |  蒸馏石油 | B. |  除去甲烷中少量乙烯 | ||
| C. |  验证化学能转变为电能 | D. |  检验乙炔的还原性 |
分析 A.温度计测定馏分的温度,冷却水下进上出;
B.乙烯被高锰酸钾氧化生成二氧化碳;
C.由图可知,构成原电池;
D.乙炔及混有的硫化氢均能被高锰酸钾氧化.
解答 解:A.温度计测定馏分的温度,冷却水下进上出,则温度计的水银球应在烧瓶的支管口处,冷水逆流,故A错误;
B.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,应选溴水、洗气,故B错误;
C.由图可知,构成原电池,可验证化学能转变为电能,故C正确;
D.乙炔及混有的硫化氢均能被高锰酸钾氧化,应选硫酸铜溶液除杂后再检验,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、混合物分离提纯、原电池、性质实验、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
18.通过NO传感器可监测汽车排放尾气中NO含量,其工作原理如图所示,下列说法正确的是( )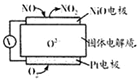

| A. | O2-向正极移动 | |
| B. | 负极的电极反应式为:NO-2e-+O2-═NO2 | |
| C. | O2的电极反应产物是H2O | |
| D. | 反应消耗的NO与O2的物质的量之比为l:2 |
10.下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A. | 金属氧化物 氧化铁 FeO | B. | 非金属氧化物 二氧化硫 SO2 | ||
| C. | 酸 次氯酸 HClO3 | D. | 碱 纯碱 Na2CO3 |
7.a、b、c、d为短周期元素,a的M电子层有l个电子,b的一种核素14b常用于鉴定文物年代,c的最高化合价与最低化合价代数和为4,d的正一价含氧酸能杀菌、消毒、漂白.下列叙述错误的是( )
| A. | 最高价含氧酸酸性:d>c>b | |
| B. | 它们均存在两种或两种以上的氧化物 | |
| C. | c 的单质难溶于水,微溶于酒精,易溶于bc2 | |
| D. | b、c、d分别与氢形成的化合物中化学键均为极性共价键 |
14.用丙醛(CH3CH2CHO)制取 的过程中发生的反应类型为( )
的过程中发生的反应类型为( )
①取代 ②消去 ③加聚 ④水解 ⑤氧化 ⑥还原.
 的过程中发生的反应类型为( )
的过程中发生的反应类型为( )①取代 ②消去 ③加聚 ④水解 ⑤氧化 ⑥还原.
| A. | ①④⑥ | B. | ⑤②③ | C. | ⑥②③ | D. | ②④⑤ |
4.Mg(OH)2在水中达到溶解平衡:Mg(OH)2(s)?Mg2+(aq)+2OH-,下列哪种情况可使Mg(OH)2(s)的量减少( )
| A. | 加入MgCl2溶液 | B. | 加入少量NaOH | C. | 加入NH4NO3溶液 | D. | 加入K2S溶液 |
11.如图是温度和压强对 X+Y?2Z反应影响示意图,下列叙述正确是( )
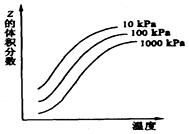

| A. | 正反应为放热 | |
| B. | 其他条件不变,升高温度,X和Y的转化率均降低 | |
| C. | X、Y、Z均为气态 | |
| D. | Z为气态,X和Y只有一种气态 |
8.除去下列物质中的杂质(括号中为杂质)只选用给出试剂(不考虑操作),正确的是( )
| A. | Al2O3(Fe2O3)用盐酸 | B. | Al2O3(SiO2)用氢氧化钠溶液 | ||
| C. | NaHCO3溶液(Na2CO3)通入过量CO2 | D. | NaHCO3溶液(Na2SiO3)通入过量CO2 |
4.在密闭容器中,将一定量A、B气体混合后发生反应:xA(g)+yB(g)?zC(g)+mD(s).平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.3mol/L.则下列有关判断正确的是( )
| A. | x+y>z+m | B. | B的转化率一定减小 | ||
| C. | 平衡向正反应方向移动 | D. | 混合气体的密度一定减小 |