题目内容
在一定温度下,反应1/2H2(g)+ 1/2X2(g)  HX(g)的平衡常数为10,若将1.0 mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于 ( )
HX(g)的平衡常数为10,若将1.0 mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于 ( )
 HX(g)的平衡常数为10,若将1.0 mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于 ( )
HX(g)的平衡常数为10,若将1.0 mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于 ( )| A.5% | B.17% | C.25% | D.33% |
B
略

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
 (正反应为放热反应),其他条件不变,则下列说法正确的一组是
(正反应为放热反应),其他条件不变,则下列说法正确的一组是 2C(g)达到平衡的标志是( )
2C(g)达到平衡的标志是( ) 2NH3已达到平衡状态的是:
2NH3已达到平衡状态的是: 4C(g)+D(s),达到平衡时C的浓度为w mol·L-1,若维持容器的体积和温度不变,按下列四种配比方案作为反应物,达平衡后,使C的浓度仍为w mol·L-1的配比是( )
4C(g)+D(s),达到平衡时C的浓度为w mol·L-1,若维持容器的体积和温度不变,按下列四种配比方案作为反应物,达平衡后,使C的浓度仍为w mol·L-1的配比是( ) 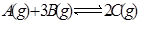 达到平衡的标志的是( )
达到平衡的标志的是( ) 2NH3(g),若维持温度和压强不变,当达到平衡时,容器的体积为V L,其中NH3的体积是0.1 V L。
2NH3(g),若维持温度和压强不变,当达到平衡时,容器的体积为V L,其中NH3的体积是0.1 V L。 2C(g) △H<0,下列各图正确的是( )
2C(g) △H<0,下列各图正确的是( )
 下反应:2A (g)+ B (g)
下反应:2A (g)+ B (g)  2C (g)。经60 s后反应达到平衡,此时容器内压强为起始时压强的0.8倍,试计算:
2C (g)。经60 s后反应达到平衡,此时容器内压强为起始时压强的0.8倍,试计算: