题目内容
绚丽的焰火将上海世博会开幕式推向了高潮.焰火与“焰色反应”知识有关.下列有关“焰色反应”的说法中正确的是( )
| A、做焰色反应实验时,用H2SO4清洗铂丝 |
| B、焰色反应是单质特有的性质 |
| C、焰色反应是化学变化 |
| D、透过蓝色钴玻璃观察,KCl与K2SO4灼烧时火焰颜色均为紫色 |
考点:焰色反应
专题:金属概论与碱元素
分析:A.H2SO4难挥发;
B.焰色反应是元素的性质;
C.焰色反应是物理变化;
D.钾元素的焰色反应的颜色为紫色,但要透过蓝色钴玻璃.
B.焰色反应是元素的性质;
C.焰色反应是物理变化;
D.钾元素的焰色反应的颜色为紫色,但要透过蓝色钴玻璃.
解答:
解:A.铂丝要用盐酸来洗涤,更容易将铂丝上的物质洗去,且盐酸易挥发不会干扰实验,故A错误;
B.焰色反应是元素的性质,不是单指,故B错误;
C.焰色反应没有新物质生成,是物理变化,故C错误;
D.钾元素的焰色反应的颜色为紫色,但要透过蓝色钴玻璃滤去火焰的黄光才能观察到,故D正确.
故选D.
B.焰色反应是元素的性质,不是单指,故B错误;
C.焰色反应没有新物质生成,是物理变化,故C错误;
D.钾元素的焰色反应的颜色为紫色,但要透过蓝色钴玻璃滤去火焰的黄光才能观察到,故D正确.
故选D.
点评:本题考查了焰色反应的一些操作细节问题,注意铂丝要用盐酸来洗涤,难度不大,注重相关基础知识的积累.

练习册系列答案
相关题目
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对生态系统造成很大的损害,其中还原沉淀法是常用的一种处理方法.流程如下下列有关说法正确的是( )
CrOH42-
Cr2O72-→
Cr3+
Cr(OH)3↓
其中第①步中存在平衡:2CrO42-(黄色)+2H+???Cr2O72-(橙色)+H2O.
CrOH42-
| H+ |
| ①转化 |
| Fe2+ |
| ②还原 |
| 沉淀剂 |
| ③沉淀 |
其中第①步中存在平衡:2CrO42-(黄色)+2H+???Cr2O72-(橙色)+H2O.
| A、第①步当2v(Cr2O72-)=v(CrO42-)时,达到了平衡状态 |
| B、对于上述平衡,加入适量稀硫酸后,溶液颜色变黄色,则有利于CrO42-的生成 |
| C、常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至9 |
| D、第②步中,还原0.1 mol Cr2O72-需要91.2 g FeSO4 |
三氟化氮(NF3)是微电子工业中一种优良的等离子蚀刻气体.它无色、无臭,在潮湿的空气中能发生反应:3NF3+5H2O═2NO+HNO3+9HF,下列有关说法正确的( )
| A、反应中NF3是氧化剂,H2O是还原剂 |
| B、反应中氧化剂与还原剂的物质的量之比为1:2 |
| C、若反应中生成0.2 mol HNO3,则反应共转移0.2 mol e- |
| D、NF3在潮湿的空气中泄漏会产生白雾、红棕色气体等现象 |
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L.向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g.再将得到的沉淀灼烧至质量不再改变为止,得到固体p g.则下列关系不正确的是( )
A、c=
| ||
B、p=m+
| ||
| C、n=m+17Vc | ||
D、
|
已知:P4(g)+6Cl2(g)═4PCl3(g),△H=a kJ?mol-1,P4(g)+10Cl2(g)═4PCl5(g),△H=b kJ?mol-1,P4具有正四面体结构,PCl5中P-Cl键的键能为c kJ?mol-1,PCl3中P-Cl键的键能为1.2c kJ?mol-1,下列叙述正确的是( )
| A、P-P键的键能大于P-Cl键的键能 | ||
| B、可求Cl2(g)+PCl3(g)=PCl5(s)的反应热△H | ||
C、Cl-Cl键的键能为
| ||
D、P-P键的键能为
|
下列所得溶液的物质的量浓度等于0.1mol?L-1的是( )
| A、将0.1 mol氨充分溶解在1 L水中 |
| B、将10 g质量分数为98%的硫酸与990 g水混合 |
| C、将8 g三氧化硫溶于水并配成1 L溶液 |
| D、将0.1 mol氧化钠溶于水并配成1 L溶液 |
用NA表示阿伏加德罗常数,1mol SO2分子中含有氧原子数为( )
| A、NA |
| B、2NA |
| C、3NA |
| D、4NA |
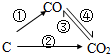 由碳元素构成的各种单质和化合物始终都是科学家研究的重要对象.
由碳元素构成的各种单质和化合物始终都是科学家研究的重要对象.