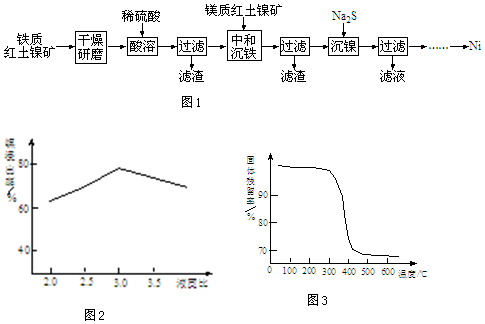
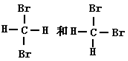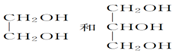题目内容
14.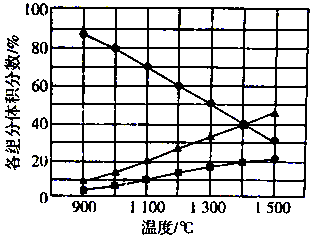 H2S在高温下分解生成硫蒸气(S2)和H2,不同温度下,反应体系中各组分的体积分数如图所示.则1400℃时反应体系中混合气体的平均摩尔质量为( )
H2S在高温下分解生成硫蒸气(S2)和H2,不同温度下,反应体系中各组分的体积分数如图所示.则1400℃时反应体系中混合气体的平均摩尔质量为( )| A. | 20.8g/mol | B. | 27.2 g/mol | C. | 33.3 g/mol | D. | 39.6 g/mol |
分析 根据题意知,该反应是可逆反应,反应物是硫化氢,根据图象知,生成物中含有S元素的物质是氢气的一半,则生成物是S2和H2,再结合反应条件书写方程式,图象中1400℃时反应体系中混合气体中各组分体积分数:H2S体积分数40%、H2体积分数40%、S2体积分数20%,气体物质的量之比2:1:2,摩尔质量等于气体质量除以总物质的量得到.
解答 解:根据题意知,该反应是可逆反应,反应物是硫化氢,根据图象知,生成物中含有S元素的物质是氢气的一半,则生成物是S2和H2,再结合反应条件书写方程式,图象中1400℃时反应体系中混合气体中各组分体积分数:H2S体积分数40%、H2体积分数40%、S2体积分数20%,气体物质的量之比2:1:2,混合气体的平均摩尔质量=$\frac{2×2+1×64+2×34}{2+1+2}$g/mol=27.2g/mol,
故选B.
点评 本题考查了化学反应电离关系和图象分析判断,依据体积分数之比等于气体物质的量之比计算得到气体物质的量之比,摩尔质量等于气体质量除以总物质的量,题目难度中等.

练习册系列答案
 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
4.下列离子方程式书写不正确的是( )
| A. | AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=7:2时,2Al3++7OH-=Al(OH)3↓+AlO2-+2H2O | |
| B. | 向饱和Na2CO3溶液中通入过量的CO2:CO32-+CO2+H2O=2HCO3- | |
| C. | CuCl2溶液与NaHS溶液反应,当n(CuCl2):n(NaHS)=1:2时,Cu2++2HS-=CuS↓+H2S↑ | |
| D. | Fe与稀硝酸反应,当n(Fe):n(HNO3)=1:2时,3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O |
5.下列项目判断,结论正确的是( )
| 选项 | 项目 | 结论 |
| A | 三种有机化合物:乙烷、氯乙烯、苯 | 分子内所有原子均在同一平面上 |
| B | C4H8Cl2的同分异构体数目(不考虑立体异构) | 共有10种 |
| C | 乙烯和苯都能使溴水褪色 | 褪色的原理相同 |
| D | 由乙酸和乙醇制乙酸乙酯,油脂水解 | 均属于取代反应 |
| A. | A | B. | B | C. | C | D. | D |
19.质量相同的下列物质,含分子数最少的是( )
| A. | 氢气 | B. | 氧气 | C. | 氮气 | D. | 二氧化碳 |
3.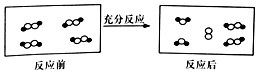 一定条件下,某容器中各微粒在反应前后变化的示意图如图,其中•和○代表不同元素的原子.关于此反应说法正确的是( )
一定条件下,某容器中各微粒在反应前后变化的示意图如图,其中•和○代表不同元素的原子.关于此反应说法正确的是( )
 一定条件下,某容器中各微粒在反应前后变化的示意图如图,其中•和○代表不同元素的原子.关于此反应说法正确的是( )
一定条件下,某容器中各微粒在反应前后变化的示意图如图,其中•和○代表不同元素的原子.关于此反应说法正确的是( )| A. | 属于化合反应 | B. | 属于置换反应 | ||
| C. | 属于氧化还原反应 | D. | 属于复分解反应 |
11.化学在工农业生产和日常生活中都有着重要的应用.下列说法错误的是( )
| A. | 利用催化设施,可以将汽车尾气中CO和NO转化为无害气体 | |
| B. | 半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 | |
| C. | 锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 | |
| D. | 防止酸雨发生的重要措施之一是使用清洁能源 |