题目内容
20.已知下表中的四个热化学方程式,| 嫦娥一号 | 液氢(H2) | ①2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ•mol-1 ②2H2(l)+O2(l)=2H2O(g)△H=-482.6kJ•mol-1 |
| 祥云火炬 | 丙烷 (C3H8) | ③C3H8(l)+5O2(g)=3CO2(g)+4H2O(g)△H=-2013.8kJ•mol-1 ④C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2221.5kJ•mol-1 |
(2)氢气作为燃料的主要优点是燃烧热值高,燃烧产物不污染环境.
分析 (1)1mol可燃物完全燃烧生成稳定氧化物放出的热量为燃烧热,结合热化学方程式分析判断和计算燃烧热进行判断;
(2)根据燃烧热值高低结合产物有无污染环境判断.
解答 解:(1)由①2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ•mol-1 ,热化学方程式是2mol氢气燃烧生成稳定氧化物的反应,则氢气的燃烧热是$\frac{571.6KJ/mol}{2}$=285.8kJ•mol-1,
②2H2(l)+O2(l)=2H2O(g)△H=-482.6kJ•mol-1,热化学方程式生成的是气体水,不是稳定氧化物,不能据此计算;
③C3H8(l)+5O2(g)=3CO2(g)+4H2O(g)△H=-2013.8kJ•mol-1,反应生成的水是气体,不是稳定氧化物,不能据此计算;
④C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2221.5kJ•mol-1,是1mol丙烷完全燃烧生成稳定氧化物放热为燃烧热即为2221.5kJ•mol-1;
故答案为:285.8 kJ•mol-1;2221.5 kJ•mol-1;
(2)根据(1)得出氢气的燃烧热是285.8kJ•mol-1,则氢气的燃烧热值为$\frac{285.8}{2}$=142.9KJ/g,丙烷燃烧热为2221.5kJ•mol-1,则丙烷燃烧热值为$\frac{2221.5}{44}$=50.49KJ/g,所以氢气作为燃料的主要优点是燃烧热值高,燃烧产物不污染环境,
故答案为:燃烧热值高,燃烧产物不污染环境.
点评 本题考查了燃烧热概念的分析理解和热化学方程式的判断应用,把握概念是解题关键,题目较简单.

练习册系列答案
相关题目
10.某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备:下列叙述错误的是( )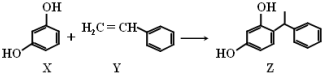

| A. | X、Y和Z均能使溴水褪色 | |
| B. | X和Z均能与Na2CO3溶液反应 | |
| C. | Y分子中所有原子可能在同一平面上 | |
| D. | Z能发生加成反应、取代反应,但不能发生氧化反应 |
11.现有NO、NO2、O3三种气体,它们含有的氧原子数目相同,则三种气体的物质的量之比为( )
| A. | 6:3:2 | B. | 3:2:1 | C. | 1:2:3 | D. | 1:1:1 |
9.下列实验过程中,始终无明显现象的是( )
| A. | CO2通入饱和Na2CO3溶液中 | B. | SO2通入Ca(ClO)2溶液中 | ||
| C. | NH3通入HNO3和AgNO3的混和溶液中 | D. | CO2通入BaCl2溶液中 |
5.实验室用乙酸和正丁醇制备乙酸正丁酯,有关物质的物理性质如表,请回答有关问题
Ⅰ.乙酸正丁酯粗产品的制备
在干燥的50mL圆底烧瓶中,装入沸石,加入11.5mL正丁醇和9.4mL冰醋酸,再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)写出乙酸正丁酯制备的化学方程式:CH3COOH+CH3CH2CH2CH2OH $?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O.本实验过程中可能产生多种有机副产物,写出其中一种的结构简式:CH2═CHCH2CH3或CH3CH2CH2CH2OCH2CH2CH2CH3.
(2)在乙酸乙酯的制备过程中采用了“边反应边蒸馏”的方式收集乙酸乙酯,乙酸正丁酯的制备过程中能否采用“边反应边蒸馏”的方式?为什么?不可以.因为乙酸正丁酯的沸点比乙酸和正丁醇都高
Ⅱ.乙酸正丁酯精产品的制备
(1)将乙酸正丁酯粗产品用如下操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用15%碳酸钠溶液洗涤,正确的操作步骤是C(填字母).
AA.①②③④B.③①④②
C.①④①③②D.④①③②③
(2)将酯层采用如图1所示装置蒸馏.
①写出图1中仪器A的名称冷凝管,冷却水从g口进入(填字母).
②蒸馏收集乙酸正丁酯产品时,应将温度控制在126.1℃左右.
Ⅲ.计算产率
(1)测量分水器内由乙酸与正丁醇反应生成水的体积为1.8mL,假设在制取乙酸正丁酯过程中反应物和生成物没有损失,且忽略副反应,计算乙酸正丁酯的产率为79.4%.实验中为了提高乙酸正丁酯的产率,采取的措施是BC
A.使用催化剂 B.加过量乙酸 C.不断移去产物 D.缩短反应时间
(2)正丁醇若含有乙醇,有同学认为制得的乙酸丁酯中含有乙酸乙酯.为了证实该观点,可尝试选用下列C(填序号)装置来做实验,请简述与实验结论有关的实验过程和现象将制得的乙酸丁酯进行蒸馏,看能否得到78℃左右的馏分,且该馏分不溶于饱和碳酸钠溶液.
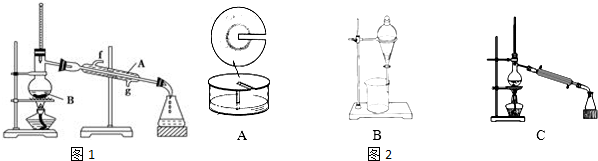
| 化合物 | 密度/g•cm-3 | 沸点/℃ | 溶解性 |
| 正丁醇 | 0.810 | 118.0 | 可溶 |
| 冰醋酸 | 1.049 | 118.1 | 互溶 |
| 乙酸正丁酯 | 0.882 | 126.1 | 微溶 |
| 乙醇 | 0.79 | 78.5 | 互溶 |
| 乙酸乙酯 | 0.88 | 77.06 | 可溶 |
在干燥的50mL圆底烧瓶中,装入沸石,加入11.5mL正丁醇和9.4mL冰醋酸,再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)写出乙酸正丁酯制备的化学方程式:CH3COOH+CH3CH2CH2CH2OH $?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O.本实验过程中可能产生多种有机副产物,写出其中一种的结构简式:CH2═CHCH2CH3或CH3CH2CH2CH2OCH2CH2CH2CH3.
(2)在乙酸乙酯的制备过程中采用了“边反应边蒸馏”的方式收集乙酸乙酯,乙酸正丁酯的制备过程中能否采用“边反应边蒸馏”的方式?为什么?不可以.因为乙酸正丁酯的沸点比乙酸和正丁醇都高
Ⅱ.乙酸正丁酯精产品的制备
(1)将乙酸正丁酯粗产品用如下操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用15%碳酸钠溶液洗涤,正确的操作步骤是C(填字母).
AA.①②③④B.③①④②
C.①④①③②D.④①③②③
(2)将酯层采用如图1所示装置蒸馏.
①写出图1中仪器A的名称冷凝管,冷却水从g口进入(填字母).
②蒸馏收集乙酸正丁酯产品时,应将温度控制在126.1℃左右.
Ⅲ.计算产率
(1)测量分水器内由乙酸与正丁醇反应生成水的体积为1.8mL,假设在制取乙酸正丁酯过程中反应物和生成物没有损失,且忽略副反应,计算乙酸正丁酯的产率为79.4%.实验中为了提高乙酸正丁酯的产率,采取的措施是BC
A.使用催化剂 B.加过量乙酸 C.不断移去产物 D.缩短反应时间
(2)正丁醇若含有乙醇,有同学认为制得的乙酸丁酯中含有乙酸乙酯.为了证实该观点,可尝试选用下列C(填序号)装置来做实验,请简述与实验结论有关的实验过程和现象将制得的乙酸丁酯进行蒸馏,看能否得到78℃左右的馏分,且该馏分不溶于饱和碳酸钠溶液.


 .
.